Кислота
Кисло́ты — химические соединения, способные отдавать катион водорода (кислоты Брёнстеда) либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса)[1].
В быту и технике под кислотами обычно подразумеваются кислоты Брёнстеда, образующие в водных растворах избыток ионов гидроксония H3O+. Присутствие этих ионов обуславливает кислый вкус растворов кислот, способность менять окраску индикаторов и, в высоких концентрациях, раздражающее действие кислот. Подвижные атомы водорода кислот способны замещаться на атомы металлов с образованием солей, содержащих катионы металлов и анионы кислотного остатка.
Содержание
Определение кислоты
История развития представлений о кислотах
 Кислоты как класс химических соединений, обладающих рядом близких свойств, известны с древнейших времён.
Кислоты как класс химических соединений, обладающих рядом близких свойств, известны с древнейших времён.
В 1778 году французский химик Антуан Лавуазье предположил, что кислотные свойства обусловлены наличием в их составе кислорода. Эта гипотеза оказалась несостоятельной, так как многие кислоты не имеют в своём составе кислорода, в то время как многие кислородсодержащие соединения не проявляют кислотных свойств. Тем не менее, именно эта гипотеза дала название кислороду как химическому элементу[2]. В 1833 году немецкий химик Юстус Либих определил кислоту как водородсодержащее соединение, в котором водород может быть замещён на металл[2].
Первую попытку создать общую теорию кислот и оснований предпринял шведский физикохимик Сванте Аррениус. В его теории, сформулированной в 1887 году, кислота определялась как соединение, диссоциирующее в водном растворе с образованием ионов водорода H+[2]. Теория Аррениуса быстро показала свою ограниченность. Во-первых, было выяснено, что невозможно представить существование несольватированного катиона Н+ в растворе; во-вторых, теория Аррениуса не учитывала влияние растворителя на кислотно-основные равновесия; наконец, теория оказалась неприменима к неводным системам[3].
Согласно сольвентной теории Франклина, созданной в 1924 году, кислотой называлось вещество, при растворении увеличивавшее число тех же катионов, которые образуются при диссоциации растворителя. Данная теория сыграла важную роль в исследовании неводных растворов кислот. Химическая теория кислот и оснований формировалась в работах А. Ганча (1917—1927). По Ганчу, кислотами называются соединения водорода, в которых последний может быть замещён на металл или неметаллический радикал с образованием соли[2].
В 1923 году появились теории кислот и оснований Брёнстеда — Лоури и Льюиса, широко применяемые в настоящее время[4].
Кислота в теории Брёнстеда — Лоури
В протонной теории кислот и оснований, выдвинутой в 1923 г. независимо и почти одновременно датским учёным Й. Брёнстедом и английским учёным Т.-М. Лоури (Лаури), кислотой называется соединение или молекулярный ион, способные отдавать протон другому химическому соединению — основанию[5]. Согласно теории Брёнстеда — Лоури, в химическом взаимодействии кислот и оснований всегда принимают участие кислота — донор протона (кислота Брёнстеда) и сопряженное с ней основание — любое соединение, способное присоединять протон (основание Брёнстеда). Поскольку основание может быть рассмотрено как продукт отщепления протона от кислоты, электрический заряд сопряженной кислоты всегда на единицу меньше, чем заряд сопряженного с ней основания. Так, например, кислоте HCl соответствует сопряженное с ней основание — хлорид-ион Cl−[6][2].
Кислота в теории Льюиса
 Согласно электронной теории, предложенной в 1923 году американским физикохимиком Г. - Н. Льюисом, кислота — это вещество, принимающее электронную пару и образующее связь с основанием Льюиса за счёт этой пары электронов[7]. Кислотами в теории Льюиса могут быть молекулы с незаполненной восьмиэлектронной оболочкой (BF3, SO3), катионы металлов-комплексообразователей (Fe2+, Zn2+), галогениды переходных металлов (TiCl4), молекулы с полярными двойными связями (SO2), карбокатионы. По сравнению с теорией Брёнстеда — Лоури, теория Льюиса является более общей и охватывает более широкий круг кислот[3][4].
Согласно электронной теории, предложенной в 1923 году американским физикохимиком Г. - Н. Льюисом, кислота — это вещество, принимающее электронную пару и образующее связь с основанием Льюиса за счёт этой пары электронов[7]. Кислотами в теории Льюиса могут быть молекулы с незаполненной восьмиэлектронной оболочкой (BF3, SO3), катионы металлов-комплексообразователей (Fe2+, Zn2+), галогениды переходных металлов (TiCl4), молекулы с полярными двойными связями (SO2), карбокатионы. По сравнению с теорией Брёнстеда — Лоури, теория Льюиса является более общей и охватывает более широкий круг кислот[3][4].
Ключевым свойством, определяющим способность взаимодействия кислоты Льюиса с основанием Льюиса, является энергетическое соответствие между низшей свободной молекулярной орбиталью, принимающей электронную пару, и высшей занятой молекулярной орбиталью, с которой эта электронная пара уходит. Эта способность была учтена в рамках принципа жёстких и мягких кислот и оснований Пирсона (принцип ЖМКО). Данный принцип устанавливает, что наиболее склонны взаимодействовать мягкие кислоты с мягкими основаниями и жёсткие кислоты с жёсткими основаниями. При этом под жёсткими кислотами понимаются кислоты Льюиса, обладающие большим положительным зарядом, большой электроотрицательностью и низкой поляризуемостью. Напротив, мягкие кислоты обладают малым положительным зарядом, низкой электроотрицательностью и высокой поляризуемостью. Поскольку данные свойства изменяются плавно, ряд кислот Льюиса занимает промежуточное положение между жёсткими и мягкими[4]. Принцип ЖМКО не имеет количественного критерия оценки силы кислот, поэтому он не может быть применён для аналитических расчётов[3].
| Жёсткие кислоты | Промежуточные кислоты | Мягкие кислоты |
|---|---|---|
| H+, Li+, Na+, K+, Mg2+, Ca2+, Al3+, Cr3+, Fe3+, BF3, B(OR)3, AlR3, AlCl3, SO3, BF3, RCO+, CO2, RSO2+ | Cu2+, Fe2+, Zn2+, SO2, R3C+, C6H5+, NO+ | Ag+, Cu+, Hg2+, RS+, I+, Br+, Pb2+, BH3, карбены |
| Жёсткие основания | Промежуточные основания | Мягкие основания |
| OH−, RO−, F−, Cl−, RCOO−, NO3−, NH3, RNH2, H2O, ROH, SO42−, CO32−, R2O, NR2−, NH2− | Br−, C6H5NH2, NO2−, C5H5N | RS−, RSH, I−, H−, R3C−, алкены, C6H6, R3P, (RO)3P |
Кислота в общей теории Усановича
В 1939 году М. И. Усанович сформулировал общую теорию кислот и оснований, согласно которой кислотой является частица, которая может отдавать катионы, в том числе протон, или присоединять анионы, в том числе электрон. Таким образом, понятие кислоты, по Усановичу, включает как кислоты Брёнстеда, так и кислоты Льюиса, а также окислители[3]. Кроме того, само понятие кислотности, как и основности, в общей теории Усановича рассматривается не как функция вещества как такового, а как роль, которую оно играет в зависимости от партнёра по реакции[9].
Классификация кислот
 Кроме подразделения на кислоты Льюиса и кислоты Брёнстеда, последние принято классифицировать по различным формальным признакам:
Кроме подразделения на кислоты Льюиса и кислоты Брёнстеда, последние принято классифицировать по различным формальным признакам:
- По силе
- Сильные — диссоциируют практически полностью, константы диссоциации больше 1·10−3 (HNO3);
- Слабые — константа диссоциации меньше 1·10−3 (уксусная кислота Kд= 1,7·10−5).
- По устойчивости
- По принадлежности к классам химических соединений
- По летучести
- По растворимости в воде
Номенклатура кислот
Номенклатура неорганических кислот
Названия кислородсодержащих кислот состоят из двух частей: собственного названия кислоты, выраженного прилагательным, и группового слова кислота (серная кислота, фосфорная кислота). Собственное название кислоты образуется от русского названия кислотообразующего элемента путём добавления различных суффиксов:
- -н-, -ов-, -ев- (если элемент находится в единственной или высшей степени окисления);
- промежуточная степень окисления +5 обозначается суффиксом -новат- (хлорноватая кислота HClO3, бромноватая кислота HBrO3, иодноватая кислота HIO3);
- промежуточные степени окисления +3 и +4 обозначаются суффиксом -(ов)ист- (мышьяковистая кислота HAsO2, хлористая кислота HClO2);
- степень окисления +1 обозначается суффиксом -новатист- (азотноватистая кислота H2N2O2, хлорноватистая кислота HClO).
Если кислотообразующий элемент в двух кислотах находится в одной и той же степени окисления, но кислоты отличаются по «содержанию воды», то для кислоты с меньшим содержанием кислорода к названию добавляют приставку мета-, а для кислоты с большим содержанием кислорода — приставку орто-, например, метафосфорная кислота HPO3 и ортофосфорная кислота H3PO4.
Кислородсодержащие кислоты с несколькими кислотообразующими элементами называются изополикислотами. Их обычно называют традиционными названиями (дифосфорная кислота H4P2O7, дисерная кислота H2S2O7).
Кислоты, в которых атомы кислорода заменены на атомы серы, называются тиокислотами и имеют соответствующую приставку тио- (тиофосфорная кислота H3PO3S). Если гидроксильные группы кислоты или атомы кислорода замещены на атомы галогенов или аминогруппу, то к названию также добавляется соответствующая приставка (амидофосфорная кислота H2PO3NH2), а замещённые серные кислоты по традиции называют сульфоновыми (хлорсульфоновая кислота ClSO3H).
Кислоты с пероксидным мостиком -O-O- относятся к пероксокислотам и имеют приставку пероксо- (пероксомоносерная кислота H2SO5) либо над- (надсерная кислота)[11].
В систематических названиях кислот к корню латинского названия кислотообразующего элемента добавляют суффикс -ат, а названия остальных элементов или их групп в анионе обозначаются приставками. В скобках указывают степень окисления кислотообразующего элемента, если она имеет целочисленное значение. В противном случае в название включают и число атомов водорода: HClO4 — тетраоксохлорат(VII) водорода (хлорная кислота), HAuCl4 — тетрахлороаурат(III) водорода (золотохлористоводородная кислота), H[Sb(OH)6] — гексагидроксостибат(V) водорода и т. д.[12]
Номенклатура органических кислот
Традиционно для простейших карбоновых кислот наиболее распространены тривиальные названия, некоторые из которых образовались ещё в XVII веке (уксусная кислота, масляная кислота, адипиновая кислота, фталевая кислота). Высшие карбоновые кислоты с чётным числом атомов углерода также имеют тривиальные названия, которые, однако, так сходны, что их употребление может вызывать путаницу (каприловая кислота, каприновая кислота).
Систематические названия карбоновых кислот образуются путём добавления окончания -овая кислота к названию соответствующего кислоте алкана (гексановая кислота, пентакозановая кислота). В случае дикарбоновых кислот используется окончание -диовая кислота (декандиовая кислота). Иногда название более удобно образовывать при помощи окончания -карбоновая кислота, которое означает замену одного атома водорода в соединении на карбоксильную группу. Такой подход применяется в тех случаях, когда карбоксильная группа присоединена к циклической системе (циклопропанкарбоновая кислота).
Если в карбоновой кислоте содержится пероксидный мостик, то к названию таких кислот добавляются приставки перокси-, пер- или над- (надуксусная кислота, пероксибензойная кислота).
Для обозначения серосодержащих органических кислот используют окончания -сульфоновая кислота (RSO3H), -сульфиновая кислота (RSO2H), -сульфеновая кислота (RSOH), аналогичным образом добавляя их к названию родоначального алкана RH[13].
| Формула | Название по ИЮПАК | Тривиальное название | Происхождение тривиального названия |
|---|---|---|---|
| НСООН | метановая кислота | муравьиная кислота | лат. formica — муравьи |
| СН3-СООН | этановая кислота | уксусная кислота | лат. acetum — уксус |
| СН3-СН2-СООН | пропановая кислота | пропионовая кислота | др.-греч. proto + pion — первый + жир |
| СН3-(СН2)2-СООН | бутановая кислота | масляная кислота | лат. butyrum — масло |
| СН3-(СН2)3-СООН | пентановая кислота | валериановая кислота | лат. Valeriána — валериана |
| СН3-(СН2)4-СООН | гексановая кислота | капроновая кислота | лат. caper — коза |
| СН3-(СН2)5-СООН | гептановая кислота | энантовая кислота | др.-греч. oenanthe — цветок винограда |
| СН3-(СН2)6-СООН | октановая кислота | каприловая кислота | лат. caper — коза |
| СН3-(СН2)7-СООН | нонановая кислота | пеларгоновая кислота | лат. Pelargonium — пеларгония |
| СН3-(СН2)8-СООН | декановая кислота | каприновая кислота | лат. caper — коза |
| СН3-(СН2)9-СООН | ундекановая кислота | ундециловая кислота | |
| СН3-(СН2)10-СООН | додекановая кислота | лауриновая кислота | лат. Laurus — лавр |
| СН3-(СН2)11-СООН | тридекановая кислота | тридециловая кислота | |
| СН3-(СН2)12-СООН | тетрадекановая кислота | миристиновая кислота | лат. Myristica — мускатный орех, др.-греч. mύρων — оливковое масло |
| СН3-(СН2)13-СООН | пентадекановая кислота | пентадециловая кислота | |
| СН3-(СН2)14-СООН | гексадекановая кислота | пальмитиновая кислота | лат. palma — пальмовое дерево |
| СН3-(СН2)15-СООН | гептадекановая кислота | маргариновая кислота | др.-греч. margaron — жемчуг |
| СН3-(СН2)16-СООН | октадекановая кислота | стеариновая кислота | др.-греч. stear — сало |
| СН3-(СН2)17-СООН | нонадекановая кислота | нонадециловая кислота | |
| С6Н5-СООН | бензолкарбоновая кислота | бензойная кислота | |
| СН2=СН-СООН | пропеновая кислота | акриловая кислота | лат. acer + olere — острый запах |
| СН≡С-СООН | пропиновая кислота | пропиоловая кислота | |
| СН3-С(СН3)2-СООН | 2,2-диметилпропановая | пивалиновая кислота | сокр. от пинаколин + валериановая кислота[К 1] |
Диссоциация и сила кислот
Количественное описание силы кислот
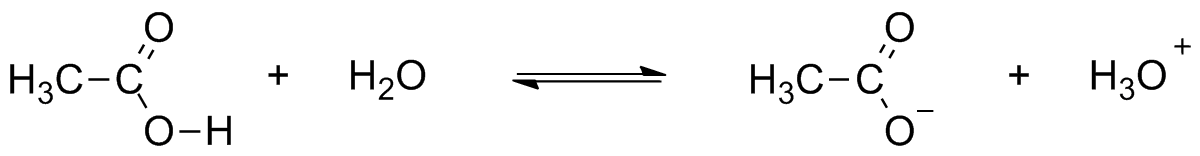
Теория кислот и оснований Брёнстеда, рассматривающая кислоту, как частицу, способную отдавать протон, даёт возможность количественно оценить эту способность кислоты — её силу. Сила кислот описывается при помощи константы равновесия реакции диссоциации кислоты в водном растворе, называемой также константой кислотности Ka. Чем больше значение Ka, тем больше способность кислоты отдавать протон и тем выше её сила. Также константа кислотности выражается в виде более удобной величины pKa — отрицательного логарифма величины Ka. Например, уравнение диссоциации и константу кислотности плавиковой кислоты можно записать следующим образом[16][17]:
<math>\mathsf{HF+H_2O}\rightleftharpoons\mathsf{H_3O^++F^-}</math>
<math>K_\mathrm{a}=\frac{[\mathsf{H_3O^+}]\cdot[\mathsf{F^-}]}{[\mathsf{HF}]} = 6{,}61\cdot10^{-4};</math>
<math>\ \mathrm{p}K_\mathrm{a}=-\log K_\mathrm{a} = 3{,}18.</math>
Для многоосновных кислот используют несколько значений констант диссоциации Ka1, Ka2 и т. д., соответствующих каждой ступени диссоциации. Например, фосфорная кислота диссоциирует по трём ступеням[17]:
<math>\mathsf{H_3PO_4+H_2O}\rightleftharpoons\mathsf{H_2PO_4^-+H_3O^+}; K_\mathrm{a1}=\frac{[\mathsf{H_2PO_4^-}]\cdot[\mathsf{H_3O^+}]}{[\mathsf{H_3PO_4}]} = 7{,}52\cdot10^{-3};</math>
<math>\mathsf{H_2PO_4^-+H_2O}\rightleftharpoons\mathsf{HPO_4^{2-}+H_3O^+}; K_\mathrm{a2}=\frac{[\mathsf{HPO_4^{2-}}]\cdot[\mathsf{H_3O^+}]}{[\mathsf{H_2PO_4^-}]} = 6{,}31\cdot10^{-8};</math>
<math>\mathsf{HPO_4^{2-}+H_2O}\rightleftharpoons\mathsf{PO_4^{3-}+H_3O^+}; K_\mathrm{a3}=\frac{[\mathsf{PO_4^{3-}}]\cdot[\mathsf{H_3O^+}]}{[\mathsf{HPO_4^{2-}}]} = 1{,}26\cdot10^{-12}.</math>
| Кислота | Значение (m — n) | Ka |
|---|---|---|
| HClO | 0 | 10−8 |
| H3AsO3 | 0 | 10−10 |
| Н2SО3 | 1 | 10−2 |
| Н3РО4 | 1 | 10−2 |
| HNO3 | 2 | 101 |
| H2SO4 | 2 | 103 |
| HClO4 | 3 | 1010 |
Кислоты принято условно подразделять по их силе на очень сильные (pKa < 0), сильные (0 < pKa < 4,5), средней силы (4,5 < pKa < 9), слабые (9 < pKa < 14), очень слабые (pKa > 14)[2].
Для приблизительной оценки силы кислот применяют эмпирические правила Полинга. Так, для неорганических кислородсодержащих кислот вида HnXOm известно эмпирическое правило, по которому значение первой константы связано со значением (m — n). Если (m — n) = 0, то кислота очень слабая, при 1 — слабая, при 2 — сильная, и, наконец, при 3 кислота очень сильная[18]. Кроме того, если такую кислоту записать в виде (HO)aXOb, выделив отдельно атомы кислорода, входящие в состав гидроксильных групп, то величину константы диссоциации по первой ступени можно оценить по уравнению:
<math>\ \mathrm{p}K_\mathrm{a1}=8-5b,</math>
то есть величина первой константы диссоциации определяется, в основном, числом негидроксильных атомов кислорода b. Эту зависимость связывают с отрицательным индуктивным влиянием этих атомов кислорода на связи O-H, за счёт которого облегчается отщепление протона от молекулы кислоты[19].
Л. Полингу также приписывают эмпирическое правило, связанное с кислотностью многоосновных кислот, которое говорит, что последовательные константы диссоциации многоосновных кислот pKa1, pKa2, pKa3 находятся в отношении 1 : 10−5 : 10−10. Уменьшение констант кислотности связано с увеличением заряда образующегося аниона[19]. Рассчитанные по правилам Полинга значения pKa отличаются от экспериментальных всего на ±1[20].
Другой характеристикой силы кислоты может служить степень диссоциации α — отношение количества диссоциированных на ионы молекул кислоты к их исходному количеству в растворе. Степень диссоциации выражается в процентах либо в виде безразмерной величины от 0 до 1[21]:
<math>\alpha=\frac{C_\text{dis}}{C_0}=\frac{[\mathsf{X^-}]}{[\mathsf{HX}]+[\mathsf{X^-}]}.</math>
| Формула кислоты | pKa | Формула кислоты | pKa |
|---|---|---|---|
| HClO4 | -5 ± 0,5 | H2PO4- | 7,20 |
| H2SO4 | -2,8 ± 0,5 | HClO | 7,25 |
| H3O+ | -1,74 | H3BO3 | 9,24 |
| HNO3 | -1,32 | NH4+ | 9,25 |
| (COOH)2 | 1,26 | HCN | 9,22 |
| H2SO3 | 1,92 | HCO3- | 10,33 |
| HSO4- | 1,96 | H2O2 | 11,62 |
| H3PO4 | 2,12 | HPO42- | 12,32 |
| HF | 3,14 | H2O | 15,74 |
| HNO2 | 3,35 | NH3 (ж.) | 33 |
| CH3COOH | 4,76 | H2 | 38,6 |
| H2S | 7,05 | СH4 | ~58 |
Влияние растворителя
Нивелирование и дифференцирование кислот
 На кислотно-основное равновесие значительное влияние оказывает растворитель. В частности, для водных растворов было обнаружено, что все кислоты с константами кислотности pKa < 0 имеют одинаковые свойства (например, pH растворов). Объясняется это тем, что для таких кислот равновесие практически нацело смещено в сторону образования иона гидроксония H3O+, который является единственной кислотой в растворе. По сути, ион гидроксония представляет собой самую сильную кислоту в водных растворах, поскольку все более сильные кислоты нацело превращаются в него и таким образом выравниваются по своей силе. Например, все кислоты с pKa < 0 (HCl, HBr, H2SO4) нацело диссоциированы в водных растворах.
На кислотно-основное равновесие значительное влияние оказывает растворитель. В частности, для водных растворов было обнаружено, что все кислоты с константами кислотности pKa < 0 имеют одинаковые свойства (например, pH растворов). Объясняется это тем, что для таких кислот равновесие практически нацело смещено в сторону образования иона гидроксония H3O+, который является единственной кислотой в растворе. По сути, ион гидроксония представляет собой самую сильную кислоту в водных растворах, поскольку все более сильные кислоты нацело превращаются в него и таким образом выравниваются по своей силе. Например, все кислоты с pKa < 0 (HCl, HBr, H2SO4) нацело диссоциированы в водных растворах.
Аналогичная ситуация наблюдается и в других растворителях: если pKa протонной кислоты в системе «кислота-растворитель» превосходит кислотность протонированного растворителя (его сопряженной кислоты), то происходит полный перенос протонов от кислоты к растворителю и единственной и наиболее сильной кислотой в растворе становятся катионы протонированного растворителя; кислотность раствора при этом определяется кислотностью сопряженной кислоты растворителя. Данное явление получило название нивелирующего эффекта растворителя[22]. Аналогичным образом, и очень слабые кислоты с pKa > 14 в водных растворах выравниваются по силе[23][24].
Кислотность протонированной уксусной кислоты CH3CO2+H2 значительно выше, чем кислотность протонированной воды H3O+, поэтому нивелирующий эффект в уксуснокислых растворах наблюдается при значительно более низких pKa кислот.
Кислоты с pKa от 0 до 14 в воде диссоциированы не полностью: их кислотные свойства в растворе зависят от значения pKa. Например, монохлоруксусная и дихлоруксусная кислоты с pKa 2,86 и 1,26 соответственно сильно отличаются по степени диссоциации (в 0,1 М растворе первая диссоциирует на 11 %, а вторая — на 52 %)[25]. В этом случае говорят о дифференцирующем эффекте растворителя. Интервал pKa, в котором кислоты дифференцированы по силе, равен показателю константы автопротолиза растворителя. Для разных растворителей этот интервал различен (14 для воды, 19 для этанола, 33 для аммиака и т. д.), соответственно, и набор дифференцированных и нивелированных кислот для них разный[26].
Если растворитель обладает основными свойствами, то в нём все кислоты становятся более сильными и большее число кислот нивелируется по силе (например, в аммиаке уксусная кислота диссоциирует нацело, хотя в водных растворах она имеет среднюю силу). Напротив, если основные свойства растворителя понижаются, то сильные кислоты могут стать слабыми, а число нивелированных кислот понижается[26]. Например, уксусная кислота служит нивелирующим растворителем для хлорной кислоты HClO4, диссоциирующей в ней нацело, и хлороводородной кислоты HCl и серной кислоты H2SO4, являющихся в уксусной кислоте слабыми[27].
Влияние диэлектрической проницаемости
На диссоциацию кислот сильное действие оказывает диэлектрическая проницаемость растворителя. Это влияние особенно заметно при сравнении двух кислот разного зарядового типа. При диссоциации нейтральной кислоты, например, фенола C6H5OH, в растворе образуются два иона. Положительно заряженные кислоты, например, ион триэтиламмония (C2H5)NH+, диссоциируют с образованием одного положительно заряженного иона. Таким образом, в первом случае после реакции число ионов увеличивается, а во втором случае это число не изменяется[28].
<math>\mathsf{C_6H_5OH+S}\rightleftharpoons\mathsf{C_6H_5O^-+SH^+}</math>
<math>\mathsf{(C_2H_5)_3NH^++S}\rightleftharpoons\mathsf{(C_2H_5)_3N+SH^+}</math>
Следовательно, переход от растворителя с высокой диэлектрической проницаемостью (более полярных) к растворителям с меньшей диэлектрической проницаемостью (менее полярным) должен сильно уменьшать силу нейтральных кислот и сравнительно мало влиять на заряженные кислоты. Так, в воде фенол в 5 раз сильнее иона триэтиламмония, однако, в метаноле фенол в 2500 раз слабее этого иона[28].
Влияние специфической сольватации анионов
Растворитель может сильно увеличивать кислотность веществ, специфически стабилизируя анионы, образующиеся в результате диссоциации.
Влияние строения кислот на их силу
Существует несколько факторов, которые определяют относительную силу органических и неорганических кислот и которые связаны со строением той или иной кислоты. Часто несколько факторов действуют одновременно, поэтому трудно предсказать их суммарное влияние. Среди наиболее значимых можно выделить следующие факторы[29].
- Индуктивный эффект (эффект поля) заместителей при кислотной группировке. Электроотрицательные заместители, обладающие отрицательным индуктивным эффектом (-I-эффектом), повышают силу кислот. Например, нитроуксусная кислота O2NCH2COOH почти в 1000 раз более сильная, чем уксусная кислота CH3COOH (pKa равны 1,68 и 4,76 соответственно). Причиной этого является стабилизирующее действие, оказываемое этими заместителями на отрицательный заряд образующегося кислотного аниона. Даже в тех случаях, когда кислота заряжена положительно, а сопряжённое основание не имеет заряда, электроотрицательные группы повышают её кислотность, поскольку они дестабилизируют молекулу кислоты, повышая величину положительного заряда. Напротив, донорные заместители, обладающие +I-эффектом, понижают силу кислот. Индуктивный эффект снижается при увеличении расстояния между кислотным центром и влияющим на него заместителем[4][29].
- Мезомерный эффект (резонансный эффект). Если в анионе, образующемся при диссоциации кислоты, отрицательный заряд распределён между несколькими атомами за счёт явления резонанса, то такой анион стабилизируется и кислотность соединения возрастает. По этой причине карбоновые кислоты — более сильные кислоты, чем соответствующие им спирты (отрицательный заряд карбоксилат-ионов распределён между двумя атомами кислорода). Подобный эффект реализуется также в фенолах, где в стабилизации отрицательного заряда сопряжённого основания принимает участие ароматическая система[4][29].
- Корреляция с расположением атомов в периодической системе. Чем выше электроотрицательность элемента, с которым связан кислотный протон, тем выше сила кислоты. По этой причине кислотность увеличивается при движении вдоль периода периодической системы слева направо. Также кислотность увеличивается при переходе по группе сверху вниз, что связано с увеличением радиуса кислотообразующего атома и, следовательно, меньшей плотностью заряда на нём, что в итоге приводит к более лёгкой диссоциации[29]:
<math>\mathsf{CH_4 < NH_3 < H_2O < HF;}</math>
<math>\mathsf{HF < HCl < HBr < HI.}</math>
- Закономерности в изменении силы кислот Льюиса также связаны с расположением центрального элемента в периодической системе химических элементов. Так, более сильными кислотами Льюиса оказываются те молекулы, которым для завершения внешнего электронного слоя недостаёт только одной электронной пары. По этой причине, например, хлорид галлия(III) GaCl3 является более сильной кислотой, чем хлорид цинка ZnCl2. Также при прочих равных условиях менее сильной является такая кислота MXn, центральный атом которой больше по размеру, что связано с ослаблением взаимодействия между положительно заряженным ядром и входящей электронной парой[29].
- Статические эффекты. В случае симметричных двухосновных кислот константа диссоциации по первой ступени в два раза больше ожидаемой, поскольку в кислоте присутствует два протона, способных к ионизации. В то же время константа диссоциации по второй ступени в два раза меньше ожидаемой, поскольку дианион дикарбоновой кислоты может присоединять протон по двум эквивалентным положением. Таким образом, соотношение Ka1/Ka2 приблизительно равно 4, что реально наблюдается для дикарбоновых кислот с удалёнными друг от друга кислотными группами[29].
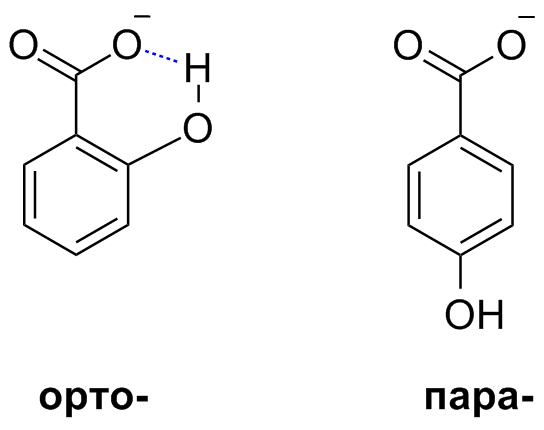
- Водородная связь. Внутримолекулярные водородные связи могут оказывать стабилизирующее влияние на образующиеся анионы и таким образом повышать силу соответствующих кислот. Так, pKa орто-гидроксибензойной кислоты составляет 2,98, а для пара-гидроксибензойной кислоты — лишь 4,58, поскольку для первого соединения возможна реализация внутримолекулярной водородной связи, а для второго нет[29].
- Пространственные эффекты. Для кислот Брёнстеда пространственные затруднения в кислотно-основных реакциях редки, поскольку протон достаточно мал. Пространственные эффекты гораздо более выражены для кислот и оснований Льюиса. Например, при использовании объёмной кислоты Льюиса Bt-Bu3 сила взаимодействия определяется не силой основания, а пространственной доступностью его электронной пары[29].
- Гибридизация. Алкины и HCN являются сравнительно более сильными кислотами, чем аналоги с двойной связью и одинарной связью, поскольку анионы при sp-гибридном атоме более устойчивы, чем при sp2- или sp3-гибридном атоме[29].
Функция кислотности Гаммета и суперкислоты
Количественную оценку кислотно-основных свойств очень сильных или концентрированных кислот невозможно провести с использованием шкалы pH, поскольку для водных растворов эта шкала ограничена снизу значением pH = 0, которому соответствует 5%-ый раствор серной кислоты H2SO4. В то же время такая необходимость возникает. Для решения данной задачи в 1932 году Л. Гамметом и А. Дейрупом была предложена функция кислотности Гаммета H0. Их подход заключался в изучении кислотно-основного равновесия очень сильных кислот в присутствии менее сильного основания, чем вода, и измерении соотношения концентраций протонированной и непротонированной форм этого основания методом электронной спектроскопии. Это дало возможность продлить шкалу кислотности в отрицательную области, благодаря чему стала возможной оценка кислотности концентрированных растворов неорганических кислот[30].
Введённая Гамметом шкала кислотности широко применяется для оценки силы суперкислот — сред с кислотностью выше, чем кислотность 100%-ой серной кислоты[31], функция кислотности Гаммета для которой составляет H0 = −12. Среди индивидуальных неорганических соединений сильными кислотами являются хлорная кислота HClO4 (H0 = −13), хлорсульфоновая кислота ClSO3H (H0 = −13,8) и фторсульфоновая кислота FSO3H (H0 = −15,1). Самой сильной из известных органических кислот является трифторметансульфокислота CF3SO3H (H0 = −14,1)[30].
К суперкислотам относятся также смеси кислот Брёнстеда и кислот Льюиса, например, смесь HF и фторида сурьмы(V) SbF5 в разных соотношениях (H0 < −30 при соотношении 1:1). Известным примером суперкислоты является олеум, где роль кислоты Льюиса выполняет SO3, который при реакции с серной кислотой даёт суперкислоту H2S2O7 (H0 = −14,5)[30].
Химические свойства кислот
- Взаимодействие с основными оксидами с образованием соли и воды:
- <math>\mathsf{CaO + 2 HCl \longrightarrow CaCl_2 + H_2O}</math>
- Взаимодействие с амфотерными оксидами с образованием соли и воды:
- <math>\mathsf{ZnO + 2 HNO_3 \longrightarrow Zn(NO_3)_2 + H_2O}</math>
- Взаимодействие со щелочами с образованием соли и воды (реакция нейтрализации):
- <math>\mathsf{NaOH + HCl \longrightarrow NaCl + H_2O}</math>
- Взаимодействие с нерастворимыми основаниями с образованием соли и воды, если используемая кислота растворима[32]:
- <math>\mathsf{Cu(OH)_2 \downarrow + H_2SO_4 \longrightarrow CuSO_4 + 2 H_2O}</math>
- <math>\mathsf{BaCl_2 + H_2SO_4 \longrightarrow BaSO_4 \downarrow + 2 HCl \uparrow}</math>
- Сильные кислоты вытесняют более слабые из их солей:
- <math>\mathsf{K_3PO_4 + 3 HCl \longrightarrow 3 KCl + H_3PO_4}</math>
- <math>\mathsf{Na_2CO_3 + 2 HCl \longrightarrow 2 NaCl + H_2O + CO_2 \uparrow}</math>
(в данном случае образуется неустойчивая угольная кислота H2CO3 , которая сразу же распадается на воду и углекислый газ)
- Металлы, стоящие в ряду активности до водорода, вытесняют его из раствора кислоты (кроме азотной кислоты HNO3 любой концентрации и концентрированной серной кислоты H2SO4), если образующаяся соль растворима:
- <math>\mathsf{Mg + 2 HCl \longrightarrow MgCl_2 + H_2 \uparrow}</math>
- С азотной кислотой и концентрированной серной кислотами реакция идёт иначе:
- <math>\mathsf{Mg + 2 H_2SO_4 \longrightarrow MgSO_4 + SO_2 \uparrow + 2 H_2O}</math>
- Для органических кислот характерна реакция этерификации (взаимодействие со спиртами с образованием сложного эфира и воды):
- <math>\mathsf{R_1-COOH + R_2-OH \longrightarrow R_1-COO-R_2 + H_2O}</math>
Например:
- <math>\mathsf{CH_3COOH + C_2H_5OH \longrightarrow CH_3COOC_2H_5 + H_2O}</math>
См. также
Напишите отзыв о статье "Кислота"
Комментарии
- ↑ Пивалиновая кислота может быть получена окислением пинаколина и изомерна валериановой кислоте.
Примечания
- ↑ [goldbook.iupac.org/A00071.html IUPAC Gold Book — Acid]. Проверено 15 апреля 2013. [www.webcitation.org/6FwKd96NK Архивировано из первоисточника 17 апреля 2013].
- ↑ 1 2 3 4 5 6 7 Химическая энциклопедия / Под ред. И. Л. Кнунянца. — М: Большая Российская энциклопедия, 1992. — Т. 2. — С. 393—395. — ISBN 5-85270-039-8.
- ↑ 1 2 3 4 Золотов Ю. А., Дорохова Е. Н., Фадеева В. И. и др. Основы аналитической химии. Книга 1. Общие вопросы. Методы разделения / Под ред. Ю. А. Золотова. — 2-е изд., перераб. и доп. — М: Высшая школа, 1999. — С. 118. — ISBN 5-06-003558-1.
- ↑ 1 2 3 4 5 6 Москва В. В. [www.pereplet.ru/nauka/Soros/pdf/9612_033.pdf Понятие кислоты и основания в органической химии] // Соросовский образовательный журнал. — 1996. — № 12. — С. 33—40.
- ↑ [goldbook.iupac.org/B00744.html IUPAC Gold Book — Brønsted acid]. Проверено 15 апреля 2013. [www.webcitation.org/6FwKdpyEJ Архивировано из первоисточника 17 апреля 2013].
- ↑ [goldbook.iupac.org/C01266.html IUPAC Gold Book — conjugate acid–base pair]. Проверено 15 апреля 2013. [www.webcitation.org/6FwKeSwog Архивировано из первоисточника 17 апреля 2013].
- ↑ [goldbook.iupac.org/L03508.html IUPAC Gold Book — Lewis acid]. Проверено 15 апреля 2013. [www.webcitation.org/6FwKf4K5a Архивировано из первоисточника 17 апреля 2013].
- ↑ Золотов и др., 1999, с. 152.
- ↑ Кусаинова К. М. [files.school-collection.edu.ru/dlrstore/d89bc7fb-0ee9-f37b-010d-ea9052b0479b/40-44_06_2004.pdf Нет ни кислот, ни оснований! Об одной полузабытой теории и её творце] // Химия и жизнь. — 2004. — № 6. — С. 40—44.
- ↑ 1 2 Рудзитис Г. Е., Фельдман Ф. Г. Химия. Неорганическая химия. 8 класс. — 15-е изд. — М: Просвещение, 2011. — С. 101. — ISBN 978-5-09-025532-5.
- ↑ Лидин Р. А., Молочко В. А., Андреева Л. Л., Цветков А. А. Основы номенклатуры неорганических веществ / Под ред. Б. Д. Степина. — М: Химия, 1983. — С. 39—45.
- ↑ Степин Б. Д. , Цветков А. А. Неорганическая химия / Под ред. Б. Д. Степина. — М: Высшая школа, 1994. — С. 18—19. — ISBN 5-06-001740-0.
- ↑ Кан Р., Дермер О. Введение в химическую номенклатуру = Introduction to Chemical Nomenclature / Пер. с англ. Н. Н. Щербиновской, под ред. В. М. Потапова и Р. А. Лидина. — М: Химия, 1983. — С. 131—134.
- ↑ Терней А. Современная органическая химия. Т. 2. — М: Мир, 1981. — С. 103.
- ↑ Senning A. Elsevier's Dictionary of Chemoetymology. The whies and whences of chemical nomenclature and terminology. — Elsevier, 2007. — 434 p. — ISBN 978-0-444-52239-9.
- ↑ Золотов и др., 1999, с. 121—122.
- ↑ 1 2 Рабинович В. А., Хавин З. Я. Краткий химический справочник. — Изд. 2-е, испр. и доп. — Ленинград: Химия, 1978. — С. 235.
- ↑ Химическая энциклопедия, 1992, т. 2, с. 396.
- ↑ 1 2 Дроздов А. А., Зломанов В. П. [www.chem.msu.su/rus/teaching/zlomanov/9.html Химия элементов главных групп периодической системы Д.И.Менделеева: галогены. 9. Свойства оксокислот хлора] (1998). Проверено 17 апреля 2013. [www.webcitation.org/6G0D4O5MP Архивировано из первоисточника 19 апреля 2013].
- ↑ Шрайвер, Эткинс, 2004, с. 244.
- ↑ Химическая энциклопедия, 1992, т. 5, с. 432.
- ↑ [pac.iupac.org/publications/pac/pdf/1979/pdf/5108x1725.pdf Levelling effect // IUPAC Glossary of terms used in physical organic chemistry. Pure & Appl. Chem., Vol. 51, p. 1768]
- ↑ Реутов и др., 2010, с. 230—232.
- ↑ Неорганическая химия / Под ред. Ю. Д. Третьякова. — М: Академия, 2004. — Т. 1. — С. 89—94. — ISBN 5-7695-1446-9.
- ↑ Реутов и др., 2010, с. 231.
- ↑ 1 2 Золотов и др., 1999, с. 123—125.
- ↑ Танганов Б. Б. [window.edu.ru/resource/575/18575/files/Niah3.pdf Химические методы анализа]. — Улан-Удэ: Издательство ВСГТУ, 2005. — С. 8—14. — ISBN 5-89230-037-4.
- ↑ 1 2 Реутов и др., 2010, с. 233.
- ↑ 1 2 3 4 5 6 7 8 9 Марч Дж. Органическая химия. Реакции, механизмы и структура. Т. 1 / Пер. с англ. З. Е. Самойловой, под ред. И. П. Белецкой. — М: Мир, 1987. — С. 340—346.
- ↑ 1 2 3 Штейнгарц В. Д. [www.pereplet.ru/nauka/Soros/pdf/9903_082.pdf Суперкислоты] // Соросовский образовательный журнал. — 1999. — № 3. — С. 82—87.
- ↑ [goldbook.iupac.org/S06135.html IUPAC Gold Book — superacid]. Проверено 23 апреля 2013. [www.webcitation.org/6GCqm6R4q Архивировано из первоисточника 28 апреля 2013].
- ↑ Мануйлов А. В., Родионов В. И. — [www.hemi.nsu.ru/ucheb183.htm Кислоты. Классификация кислот. Химические свойства.] // Основы химии. Интернет-учебник.
Литература
- Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия. — 3-е изд. — М: Бином. Лаборатория знаний, 2010. — Т. 1. — 567 с. — ISBN 978-5-94774-613-6.
- Шрайвер Д., Эткинс П. Неорганическая химия = Inorganic Chemistry / Пер. с англ. М. Г. Розовой, С. Я. Истомина, М. Е. Тамм, под ред. В. П. Зломанова. — М: Мир, 2004. — Т. 1. — 679 с. — ISBN 5-03-003628-8.
Ссылки
- [www.hemi.nsu.ru/ucheb183.htm Все о кислотах]
- [www.biochemical.com.ua/chemical-reagents1.html Органические и неорганические кислоты]
- [univertv.ru/video/himiya/obwaya_himiya/kisloty/?mark=all Кислоты: бескислородные и кислородосодержащие, соли бескислородных и кислородсодержащих кислот, типы химических реакций]
Отрывок, характеризующий Кислота
– Oui, Sire. [Да, государь.]– Mais le riz? [Но рис?]
Рапп отвечал, что он передал приказанья государя о рисе, но Наполеон недовольно покачал головой, как будто он не верил, чтобы приказание его было исполнено. Слуга вошел с пуншем. Наполеон велел подать другой стакан Раппу и молча отпивал глотки из своего.
– У меня нет ни вкуса, ни обоняния, – сказал он, принюхиваясь к стакану. – Этот насморк надоел мне. Они толкуют про медицину. Какая медицина, когда они не могут вылечить насморка? Корвизар дал мне эти пастильки, но они ничего не помогают. Что они могут лечить? Лечить нельзя. Notre corps est une machine a vivre. Il est organise pour cela, c'est sa nature; laissez y la vie a son aise, qu'elle s'y defende elle meme: elle fera plus que si vous la paralysiez en l'encombrant de remedes. Notre corps est comme une montre parfaite qui doit aller un certain temps; l'horloger n'a pas la faculte de l'ouvrir, il ne peut la manier qu'a tatons et les yeux bandes. Notre corps est une machine a vivre, voila tout. [Наше тело есть машина для жизни. Оно для этого устроено. Оставьте в нем жизнь в покое, пускай она сама защищается, она больше сделает одна, чем когда вы ей будете мешать лекарствами. Наше тело подобно часам, которые должны идти известное время; часовщик не может открыть их и только ощупью и с завязанными глазами может управлять ими. Наше тело есть машина для жизни. Вот и все.] – И как будто вступив на путь определений, definitions, которые любил Наполеон, он неожиданно сделал новое определение. – Вы знаете ли, Рапп, что такое военное искусство? – спросил он. – Искусство быть сильнее неприятеля в известный момент. Voila tout. [Вот и все.]
Рапп ничего не ответил.
– Demainnous allons avoir affaire a Koutouzoff! [Завтра мы будем иметь дело с Кутузовым!] – сказал Наполеон. – Посмотрим! Помните, в Браунау он командовал армией и ни разу в три недели не сел на лошадь, чтобы осмотреть укрепления. Посмотрим!
Он поглядел на часы. Было еще только четыре часа. Спать не хотелось, пунш был допит, и делать все таки было нечего. Он встал, прошелся взад и вперед, надел теплый сюртук и шляпу и вышел из палатки. Ночь была темная и сырая; чуть слышная сырость падала сверху. Костры не ярко горели вблизи, во французской гвардии, и далеко сквозь дым блестели по русской линии. Везде было тихо, и ясно слышались шорох и топот начавшегося уже движения французских войск для занятия позиции.
Наполеон прошелся перед палаткой, посмотрел на огни, прислушался к топоту и, проходя мимо высокого гвардейца в мохнатой шапке, стоявшего часовым у его палатки и, как черный столб, вытянувшегося при появлении императора, остановился против него.
– С которого года в службе? – спросил он с той привычной аффектацией грубой и ласковой воинственности, с которой он всегда обращался с солдатами. Солдат отвечал ему.
– Ah! un des vieux! [А! из стариков!] Получили рис в полк?
– Получили, ваше величество.
Наполеон кивнул головой и отошел от него.
В половине шестого Наполеон верхом ехал к деревне Шевардину.
Начинало светать, небо расчистило, только одна туча лежала на востоке. Покинутые костры догорали в слабом свете утра.
Вправо раздался густой одинокий пушечный выстрел, пронесся и замер среди общей тишины. Прошло несколько минут. Раздался второй, третий выстрел, заколебался воздух; четвертый, пятый раздались близко и торжественно где то справа.
Еще не отзвучали первые выстрелы, как раздались еще другие, еще и еще, сливаясь и перебивая один другой.
Наполеон подъехал со свитой к Шевардинскому редуту и слез с лошади. Игра началась.
Вернувшись от князя Андрея в Горки, Пьер, приказав берейтору приготовить лошадей и рано утром разбудить его, тотчас же заснул за перегородкой, в уголке, который Борис уступил ему.
Когда Пьер совсем очнулся на другое утро, в избе уже никого не было. Стекла дребезжали в маленьких окнах. Берейтор стоял, расталкивая его.
– Ваше сиятельство, ваше сиятельство, ваше сиятельство… – упорно, не глядя на Пьера и, видимо, потеряв надежду разбудить его, раскачивая его за плечо, приговаривал берейтор.
– Что? Началось? Пора? – заговорил Пьер, проснувшись.
– Изволите слышать пальбу, – сказал берейтор, отставной солдат, – уже все господа повышли, сами светлейшие давно проехали.
Пьер поспешно оделся и выбежал на крыльцо. На дворе было ясно, свежо, росисто и весело. Солнце, только что вырвавшись из за тучи, заслонявшей его, брызнуло до половины переломленными тучей лучами через крыши противоположной улицы, на покрытую росой пыль дороги, на стены домов, на окна забора и на лошадей Пьера, стоявших у избы. Гул пушек яснее слышался на дворе. По улице прорысил адъютант с казаком.
– Пора, граф, пора! – прокричал адъютант.
Приказав вести за собой лошадь, Пьер пошел по улице к кургану, с которого он вчера смотрел на поле сражения. На кургане этом была толпа военных, и слышался французский говор штабных, и виднелась седая голова Кутузова с его белой с красным околышем фуражкой и седым затылком, утонувшим в плечи. Кутузов смотрел в трубу вперед по большой дороге.
Войдя по ступенькам входа на курган, Пьер взглянул впереди себя и замер от восхищенья перед красотою зрелища. Это была та же панорама, которою он любовался вчера с этого кургана; но теперь вся эта местность была покрыта войсками и дымами выстрелов, и косые лучи яркого солнца, поднимавшегося сзади, левее Пьера, кидали на нее в чистом утреннем воздухе пронизывающий с золотым и розовым оттенком свет и темные, длинные тени. Дальние леса, заканчивающие панораму, точно высеченные из какого то драгоценного желто зеленого камня, виднелись своей изогнутой чертой вершин на горизонте, и между ними за Валуевым прорезывалась большая Смоленская дорога, вся покрытая войсками. Ближе блестели золотые поля и перелески. Везде – спереди, справа и слева – виднелись войска. Все это было оживленно, величественно и неожиданно; но то, что более всего поразило Пьера, – это был вид самого поля сражения, Бородина и лощины над Колочею по обеим сторонам ее.
Над Колочею, в Бородине и по обеим сторонам его, особенно влево, там, где в болотистых берегах Во йна впадает в Колочу, стоял тот туман, который тает, расплывается и просвечивает при выходе яркого солнца и волшебно окрашивает и очерчивает все виднеющееся сквозь него. К этому туману присоединялся дым выстрелов, и по этому туману и дыму везде блестели молнии утреннего света – то по воде, то по росе, то по штыкам войск, толпившихся по берегам и в Бородине. Сквозь туман этот виднелась белая церковь, кое где крыши изб Бородина, кое где сплошные массы солдат, кое где зеленые ящики, пушки. И все это двигалось или казалось движущимся, потому что туман и дым тянулись по всему этому пространству. Как в этой местности низов около Бородина, покрытых туманом, так и вне его, выше и особенно левее по всей линии, по лесам, по полям, в низах, на вершинах возвышений, зарождались беспрестанно сами собой, из ничего, пушечные, то одинокие, то гуртовые, то редкие, то частые клубы дымов, которые, распухая, разрастаясь, клубясь, сливаясь, виднелись по всему этому пространству.
Эти дымы выстрелов и, странно сказать, звуки их производили главную красоту зрелища.
Пуфф! – вдруг виднелся круглый, плотный, играющий лиловым, серым и молочно белым цветами дым, и бумм! – раздавался через секунду звук этого дыма.
«Пуф пуф» – поднимались два дыма, толкаясь и сливаясь; и «бум бум» – подтверждали звуки то, что видел глаз.
Пьер оглядывался на первый дым, который он оставил округлым плотным мячиком, и уже на месте его были шары дыма, тянущегося в сторону, и пуф… (с остановкой) пуф пуф – зарождались еще три, еще четыре, и на каждый, с теми же расстановками, бум… бум бум бум – отвечали красивые, твердые, верные звуки. Казалось то, что дымы эти бежали, то, что они стояли, и мимо них бежали леса, поля и блестящие штыки. С левой стороны, по полям и кустам, беспрестанно зарождались эти большие дымы с своими торжественными отголосками, и ближе еще, по низам и лесам, вспыхивали маленькие, не успевавшие округляться дымки ружей и точно так же давали свои маленькие отголоски. Трах та та тах – трещали ружья хотя и часто, но неправильно и бедно в сравнении с орудийными выстрелами.
Пьеру захотелось быть там, где были эти дымы, эти блестящие штыки и пушки, это движение, эти звуки. Он оглянулся на Кутузова и на его свиту, чтобы сверить свое впечатление с другими. Все точно так же, как и он, и, как ему казалось, с тем же чувством смотрели вперед, на поле сражения. На всех лицах светилась теперь та скрытая теплота (chaleur latente) чувства, которое Пьер замечал вчера и которое он понял совершенно после своего разговора с князем Андреем.
– Поезжай, голубчик, поезжай, Христос с тобой, – говорил Кутузов, не спуская глаз с поля сражения, генералу, стоявшему подле него.
Выслушав приказание, генерал этот прошел мимо Пьера, к сходу с кургана.
– К переправе! – холодно и строго сказал генерал в ответ на вопрос одного из штабных, куда он едет. «И я, и я», – подумал Пьер и пошел по направлению за генералом.
Генерал садился на лошадь, которую подал ему казак. Пьер подошел к своему берейтору, державшему лошадей. Спросив, которая посмирнее, Пьер взлез на лошадь, схватился за гриву, прижал каблуки вывернутых ног к животу лошади и, чувствуя, что очки его спадают и что он не в силах отвести рук от гривы и поводьев, поскакал за генералом, возбуждая улыбки штабных, с кургана смотревших на него.
Генерал, за которым скакал Пьер, спустившись под гору, круто повернул влево, и Пьер, потеряв его из вида, вскакал в ряды пехотных солдат, шедших впереди его. Он пытался выехать из них то вправо, то влево; но везде были солдаты, с одинаково озабоченными лицами, занятыми каким то невидным, но, очевидно, важным делом. Все с одинаково недовольно вопросительным взглядом смотрели на этого толстого человека в белой шляпе, неизвестно для чего топчущего их своею лошадью.
– Чего ездит посерёд батальона! – крикнул на него один. Другой толконул прикладом его лошадь, и Пьер, прижавшись к луке и едва удерживая шарахнувшуюся лошадь, выскакал вперед солдат, где было просторнее.
Впереди его был мост, а у моста, стреляя, стояли другие солдаты. Пьер подъехал к ним. Сам того не зная, Пьер заехал к мосту через Колочу, который был между Горками и Бородиным и который в первом действии сражения (заняв Бородино) атаковали французы. Пьер видел, что впереди его был мост и что с обеих сторон моста и на лугу, в тех рядах лежащего сена, которые он заметил вчера, в дыму что то делали солдаты; но, несмотря на неумолкающую стрельбу, происходившую в этом месте, он никак не думал, что тут то и было поле сражения. Он не слыхал звуков пуль, визжавших со всех сторон, и снарядов, перелетавших через него, не видал неприятеля, бывшего на той стороне реки, и долго не видал убитых и раненых, хотя многие падали недалеко от него. С улыбкой, не сходившей с его лица, он оглядывался вокруг себя.
– Что ездит этот перед линией? – опять крикнул на него кто то.
– Влево, вправо возьми, – кричали ему. Пьер взял вправо и неожиданно съехался с знакомым ему адъютантом генерала Раевского. Адъютант этот сердито взглянул на Пьера, очевидно, сбираясь тоже крикнуть на него, но, узнав его, кивнул ему головой.
– Вы как тут? – проговорил он и поскакал дальше.
Пьер, чувствуя себя не на своем месте и без дела, боясь опять помешать кому нибудь, поскакал за адъютантом.
– Это здесь, что же? Можно мне с вами? – спрашивал он.
– Сейчас, сейчас, – отвечал адъютант и, подскакав к толстому полковнику, стоявшему на лугу, что то передал ему и тогда уже обратился к Пьеру.
– Вы зачем сюда попали, граф? – сказал он ему с улыбкой. – Все любопытствуете?
– Да, да, – сказал Пьер. Но адъютант, повернув лошадь, ехал дальше.
– Здесь то слава богу, – сказал адъютант, – но на левом фланге у Багратиона ужасная жарня идет.
– Неужели? – спросил Пьер. – Это где же?
– Да вот поедемте со мной на курган, от нас видно. А у нас на батарее еще сносно, – сказал адъютант. – Что ж, едете?
– Да, я с вами, – сказал Пьер, глядя вокруг себя и отыскивая глазами своего берейтора. Тут только в первый раз Пьер увидал раненых, бредущих пешком и несомых на носилках. На том самом лужке с пахучими рядами сена, по которому он проезжал вчера, поперек рядов, неловко подвернув голову, неподвижно лежал один солдат с свалившимся кивером. – А этого отчего не подняли? – начал было Пьер; но, увидав строгое лицо адъютанта, оглянувшегося в ту же сторону, он замолчал.
Пьер не нашел своего берейтора и вместе с адъютантом низом поехал по лощине к кургану Раевского. Лошадь Пьера отставала от адъютанта и равномерно встряхивала его.
– Вы, видно, не привыкли верхом ездить, граф? – спросил адъютант.
– Нет, ничего, но что то она прыгает очень, – с недоуменьем сказал Пьер.
– Ээ!.. да она ранена, – сказал адъютант, – правая передняя, выше колена. Пуля, должно быть. Поздравляю, граф, – сказал он, – le bapteme de feu [крещение огнем].
Проехав в дыму по шестому корпусу, позади артиллерии, которая, выдвинутая вперед, стреляла, оглушая своими выстрелами, они приехали к небольшому лесу. В лесу было прохладно, тихо и пахло осенью. Пьер и адъютант слезли с лошадей и пешком вошли на гору.
– Здесь генерал? – спросил адъютант, подходя к кургану.
– Сейчас были, поехали сюда, – указывая вправо, отвечали ему.
Адъютант оглянулся на Пьера, как бы не зная, что ему теперь с ним делать.
– Не беспокойтесь, – сказал Пьер. – Я пойду на курган, можно?
– Да пойдите, оттуда все видно и не так опасно. А я заеду за вами.
Пьер пошел на батарею, и адъютант поехал дальше. Больше они не видались, и уже гораздо после Пьер узнал, что этому адъютанту в этот день оторвало руку.
Курган, на который вошел Пьер, был то знаменитое (потом известное у русских под именем курганной батареи, или батареи Раевского, а у французов под именем la grande redoute, la fatale redoute, la redoute du centre [большого редута, рокового редута, центрального редута] место, вокруг которого положены десятки тысяч людей и которое французы считали важнейшим пунктом позиции.
Редут этот состоял из кургана, на котором с трех сторон были выкопаны канавы. В окопанном канавами место стояли десять стрелявших пушек, высунутых в отверстие валов.
В линию с курганом стояли с обеих сторон пушки, тоже беспрестанно стрелявшие. Немного позади пушек стояли пехотные войска. Входя на этот курган, Пьер никак не думал, что это окопанное небольшими канавами место, на котором стояло и стреляло несколько пушек, было самое важное место в сражении.
Пьеру, напротив, казалось, что это место (именно потому, что он находился на нем) было одно из самых незначительных мест сражения.
Войдя на курган, Пьер сел в конце канавы, окружающей батарею, и с бессознательно радостной улыбкой смотрел на то, что делалось вокруг него. Изредка Пьер все с той же улыбкой вставал и, стараясь не помешать солдатам, заряжавшим и накатывавшим орудия, беспрестанно пробегавшим мимо него с сумками и зарядами, прохаживался по батарее. Пушки с этой батареи беспрестанно одна за другой стреляли, оглушая своими звуками и застилая всю окрестность пороховым дымом.
В противность той жуткости, которая чувствовалась между пехотными солдатами прикрытия, здесь, на батарее, где небольшое количество людей, занятых делом, бело ограничено, отделено от других канавой, – здесь чувствовалось одинаковое и общее всем, как бы семейное оживление.
Появление невоенной фигуры Пьера в белой шляпе сначала неприятно поразило этих людей. Солдаты, проходя мимо его, удивленно и даже испуганно косились на его фигуру. Старший артиллерийский офицер, высокий, с длинными ногами, рябой человек, как будто для того, чтобы посмотреть на действие крайнего орудия, подошел к Пьеру и любопытно посмотрел на него.
Молоденький круглолицый офицерик, еще совершенный ребенок, очевидно, только что выпущенный из корпуса, распоряжаясь весьма старательно порученными ему двумя пушками, строго обратился к Пьеру.
– Господин, позвольте вас попросить с дороги, – сказал он ему, – здесь нельзя.
Солдаты неодобрительно покачивали головами, глядя на Пьера. Но когда все убедились, что этот человек в белой шляпе не только не делал ничего дурного, но или смирно сидел на откосе вала, или с робкой улыбкой, учтиво сторонясь перед солдатами, прохаживался по батарее под выстрелами так же спокойно, как по бульвару, тогда понемногу чувство недоброжелательного недоуменья к нему стало переходить в ласковое и шутливое участие, подобное тому, которое солдаты имеют к своим животным: собакам, петухам, козлам и вообще животным, живущим при воинских командах. Солдаты эти сейчас же мысленно приняли Пьера в свою семью, присвоили себе и дали ему прозвище. «Наш барин» прозвали его и про него ласково смеялись между собой.
Одно ядро взрыло землю в двух шагах от Пьера. Он, обчищая взбрызнутую ядром землю с платья, с улыбкой оглянулся вокруг себя.
– И как это вы не боитесь, барин, право! – обратился к Пьеру краснорожий широкий солдат, оскаливая крепкие белые зубы.
– А ты разве боишься? – спросил Пьер.
– А то как же? – отвечал солдат. – Ведь она не помилует. Она шмякнет, так кишки вон. Нельзя не бояться, – сказал он, смеясь.
Несколько солдат с веселыми и ласковыми лицами остановились подле Пьера. Они как будто не ожидали того, чтобы он говорил, как все, и это открытие обрадовало их.
– Наше дело солдатское. А вот барин, так удивительно. Вот так барин!
– По местам! – крикнул молоденький офицер на собравшихся вокруг Пьера солдат. Молоденький офицер этот, видимо, исполнял свою должность в первый или во второй раз и потому с особенной отчетливостью и форменностью обращался и с солдатами и с начальником.
Перекатная пальба пушек и ружей усиливалась по всему полю, в особенности влево, там, где были флеши Багратиона, но из за дыма выстрелов с того места, где был Пьер, нельзя было почти ничего видеть. Притом, наблюдения за тем, как бы семейным (отделенным от всех других) кружком людей, находившихся на батарее, поглощали все внимание Пьера. Первое его бессознательно радостное возбуждение, произведенное видом и звуками поля сражения, заменилось теперь, в особенности после вида этого одиноко лежащего солдата на лугу, другим чувством. Сидя теперь на откосе канавы, он наблюдал окружавшие его лица.
К десяти часам уже человек двадцать унесли с батареи; два орудия были разбиты, чаще и чаще на батарею попадали снаряды и залетали, жужжа и свистя, дальние пули. Но люди, бывшие на батарее, как будто не замечали этого; со всех сторон слышался веселый говор и шутки.
– Чиненка! – кричал солдат на приближающуюся, летевшую со свистом гранату. – Не сюда! К пехотным! – с хохотом прибавлял другой, заметив, что граната перелетела и попала в ряды прикрытия.
– Что, знакомая? – смеялся другой солдат на присевшего мужика под пролетевшим ядром.
Несколько солдат собрались у вала, разглядывая то, что делалось впереди.
– И цепь сняли, видишь, назад прошли, – говорили они, указывая через вал.
– Свое дело гляди, – крикнул на них старый унтер офицер. – Назад прошли, значит, назади дело есть. – И унтер офицер, взяв за плечо одного из солдат, толкнул его коленкой. Послышался хохот.
– К пятому орудию накатывай! – кричали с одной стороны.
– Разом, дружнее, по бурлацки, – слышались веселые крики переменявших пушку.
– Ай, нашему барину чуть шляпку не сбила, – показывая зубы, смеялся на Пьера краснорожий шутник. – Эх, нескладная, – укоризненно прибавил он на ядро, попавшее в колесо и ногу человека.
– Ну вы, лисицы! – смеялся другой на изгибающихся ополченцев, входивших на батарею за раненым.
– Аль не вкусна каша? Ах, вороны, заколянились! – кричали на ополченцев, замявшихся перед солдатом с оторванной ногой.
– Тое кое, малый, – передразнивали мужиков. – Страсть не любят.
Пьер замечал, как после каждого попавшего ядра, после каждой потери все более и более разгоралось общее оживление.
Как из придвигающейся грозовой тучи, чаще и чаще, светлее и светлее вспыхивали на лицах всех этих людей (как бы в отпор совершающегося) молнии скрытого, разгорающегося огня.
Пьер не смотрел вперед на поле сражения и не интересовался знать о том, что там делалось: он весь был поглощен в созерцание этого, все более и более разгорающегося огня, который точно так же (он чувствовал) разгорался и в его душе.
В десять часов пехотные солдаты, бывшие впереди батареи в кустах и по речке Каменке, отступили. С батареи видно было, как они пробегали назад мимо нее, неся на ружьях раненых. Какой то генерал со свитой вошел на курган и, поговорив с полковником, сердито посмотрев на Пьера, сошел опять вниз, приказав прикрытию пехоты, стоявшему позади батареи, лечь, чтобы менее подвергаться выстрелам. Вслед за этим в рядах пехоты, правее батареи, послышался барабан, командные крики, и с батареи видно было, как ряды пехоты двинулись вперед.
Пьер смотрел через вал. Одно лицо особенно бросилось ему в глаза. Это был офицер, который с бледным молодым лицом шел задом, неся опущенную шпагу, и беспокойно оглядывался.
Ряды пехотных солдат скрылись в дыму, послышался их протяжный крик и частая стрельба ружей. Через несколько минут толпы раненых и носилок прошли оттуда. На батарею еще чаще стали попадать снаряды. Несколько человек лежали неубранные. Около пушек хлопотливее и оживленнее двигались солдаты. Никто уже не обращал внимания на Пьера. Раза два на него сердито крикнули за то, что он был на дороге. Старший офицер, с нахмуренным лицом, большими, быстрыми шагами переходил от одного орудия к другому. Молоденький офицерик, еще больше разрумянившись, еще старательнее командовал солдатами. Солдаты подавали заряды, поворачивались, заряжали и делали свое дело с напряженным щегольством. Они на ходу подпрыгивали, как на пружинах.
Грозовая туча надвинулась, и ярко во всех лицах горел тот огонь, за разгоранием которого следил Пьер. Он стоял подле старшего офицера. Молоденький офицерик подбежал, с рукой к киверу, к старшему.
– Имею честь доложить, господин полковник, зарядов имеется только восемь, прикажете ли продолжать огонь? – спросил он.
– Картечь! – не отвечая, крикнул старший офицер, смотревший через вал.
Вдруг что то случилось; офицерик ахнул и, свернувшись, сел на землю, как на лету подстреленная птица. Все сделалось странно, неясно и пасмурно в глазах Пьера.
Одно за другим свистели ядра и бились в бруствер, в солдат, в пушки. Пьер, прежде не слыхавший этих звуков, теперь только слышал одни эти звуки. Сбоку батареи, справа, с криком «ура» бежали солдаты не вперед, а назад, как показалось Пьеру.
Ядро ударило в самый край вала, перед которым стоял Пьер, ссыпало землю, и в глазах его мелькнул черный мячик, и в то же мгновенье шлепнуло во что то. Ополченцы, вошедшие было на батарею, побежали назад.
– Все картечью! – кричал офицер.
Унтер офицер подбежал к старшему офицеру и испуганным шепотом (как за обедом докладывает дворецкий хозяину, что нет больше требуемого вина) сказал, что зарядов больше не было.
– Разбойники, что делают! – закричал офицер, оборачиваясь к Пьеру. Лицо старшего офицера было красно и потно, нахмуренные глаза блестели. – Беги к резервам, приводи ящики! – крикнул он, сердито обходя взглядом Пьера и обращаясь к своему солдату.
– Я пойду, – сказал Пьер. Офицер, не отвечая ему, большими шагами пошел в другую сторону.
– Не стрелять… Выжидай! – кричал он.
Солдат, которому приказано было идти за зарядами, столкнулся с Пьером.
– Эх, барин, не место тебе тут, – сказал он и побежал вниз. Пьер побежал за солдатом, обходя то место, на котором сидел молоденький офицерик.
Одно, другое, третье ядро пролетало над ним, ударялось впереди, с боков, сзади. Пьер сбежал вниз. «Куда я?» – вдруг вспомнил он, уже подбегая к зеленым ящикам. Он остановился в нерешительности, идти ему назад или вперед. Вдруг страшный толчок откинул его назад, на землю. В то же мгновенье блеск большого огня осветил его, и в то же мгновенье раздался оглушающий, зазвеневший в ушах гром, треск и свист.
Пьер, очнувшись, сидел на заду, опираясь руками о землю; ящика, около которого он был, не было; только валялись зеленые обожженные доски и тряпки на выжженной траве, и лошадь, трепля обломками оглобель, проскакала от него, а другая, так же как и сам Пьер, лежала на земле и пронзительно, протяжно визжала.
Пьер, не помня себя от страха, вскочил и побежал назад на батарею, как на единственное убежище от всех ужасов, окружавших его.
В то время как Пьер входил в окоп, он заметил, что на батарее выстрелов не слышно было, но какие то люди что то делали там. Пьер не успел понять того, какие это были люди. Он увидел старшего полковника, задом к нему лежащего на валу, как будто рассматривающего что то внизу, и видел одного, замеченного им, солдата, который, прорываясь вперед от людей, державших его за руку, кричал: «Братцы!» – и видел еще что то странное.
Но он не успел еще сообразить того, что полковник был убит, что кричавший «братцы!» был пленный, что в глазах его был заколон штыком в спину другой солдат. Едва он вбежал в окоп, как худощавый, желтый, с потным лицом человек в синем мундире, со шпагой в руке, набежал на него, крича что то. Пьер, инстинктивно обороняясь от толчка, так как они, не видав, разбежались друг против друга, выставил руки и схватил этого человека (это был французский офицер) одной рукой за плечо, другой за гордо. Офицер, выпустив шпагу, схватил Пьера за шиворот.
Несколько секунд они оба испуганными глазами смотрели на чуждые друг другу лица, и оба были в недоумении о том, что они сделали и что им делать. «Я ли взят в плен или он взят в плен мною? – думал каждый из них. Но, очевидно, французский офицер более склонялся к мысли, что в плен взят он, потому что сильная рука Пьера, движимая невольным страхом, все крепче и крепче сжимала его горло. Француз что то хотел сказать, как вдруг над самой головой их низко и страшно просвистело ядро, и Пьеру показалось, что голова французского офицера оторвана: так быстро он согнул ее.
Пьер тоже нагнул голову и отпустил руки. Не думая более о том, кто кого взял в плен, француз побежал назад на батарею, а Пьер под гору, спотыкаясь на убитых и раненых, которые, казалось ему, ловят его за ноги. Но не успел он сойти вниз, как навстречу ему показались плотные толпы бегущих русских солдат, которые, падая, спотыкаясь и крича, весело и бурно бежали на батарею. (Это была та атака, которую себе приписывал Ермолов, говоря, что только его храбрости и счастью возможно было сделать этот подвиг, и та атака, в которой он будто бы кидал на курган Георгиевские кресты, бывшие у него в кармане.)
Французы, занявшие батарею, побежали. Наши войска с криками «ура» так далеко за батарею прогнали французов, что трудно было остановить их.
С батареи свезли пленных, в том числе раненого французского генерала, которого окружили офицеры. Толпы раненых, знакомых и незнакомых Пьеру, русских и французов, с изуродованными страданием лицами, шли, ползли и на носилках неслись с батареи. Пьер вошел на курган, где он провел более часа времени, и из того семейного кружка, который принял его к себе, он не нашел никого. Много было тут мертвых, незнакомых ему. Но некоторых он узнал. Молоденький офицерик сидел, все так же свернувшись, у края вала, в луже крови. Краснорожий солдат еще дергался, но его не убирали.
Пьер побежал вниз.
«Нет, теперь они оставят это, теперь они ужаснутся того, что они сделали!» – думал Пьер, бесцельно направляясь за толпами носилок, двигавшихся с поля сражения.
Но солнце, застилаемое дымом, стояло еще высоко, и впереди, и в особенности налево у Семеновского, кипело что то в дыму, и гул выстрелов, стрельба и канонада не только не ослабевали, но усиливались до отчаянности, как человек, который, надрываясь, кричит из последних сил.
Главное действие Бородинского сражения произошло на пространстве тысячи сажен между Бородиным и флешами Багратиона. (Вне этого пространства с одной стороны была сделана русскими в половине дня демонстрация кавалерией Уварова, с другой стороны, за Утицей, было столкновение Понятовского с Тучковым; но это были два отдельные и слабые действия в сравнении с тем, что происходило в середине поля сражения.) На поле между Бородиным и флешами, у леса, на открытом и видном с обеих сторон протяжении, произошло главное действие сражения, самым простым, бесхитростным образом.
Сражение началось канонадой с обеих сторон из нескольких сотен орудий.
Потом, когда дым застлал все поле, в этом дыму двинулись (со стороны французов) справа две дивизии, Дессе и Компана, на флеши, и слева полки вице короля на Бородино.
От Шевардинского редута, на котором стоял Наполеон, флеши находились на расстоянии версты, а Бородино более чем в двух верстах расстояния по прямой линии, и поэтому Наполеон не мог видеть того, что происходило там, тем более что дым, сливаясь с туманом, скрывал всю местность. Солдаты дивизии Дессе, направленные на флеши, были видны только до тех пор, пока они не спустились под овраг, отделявший их от флеш. Как скоро они спустились в овраг, дым выстрелов орудийных и ружейных на флешах стал так густ, что застлал весь подъем той стороны оврага. Сквозь дым мелькало там что то черное – вероятно, люди, и иногда блеск штыков. Но двигались ли они или стояли, были ли это французы или русские, нельзя было видеть с Шевардинского редута.
Солнце взошло светло и било косыми лучами прямо в лицо Наполеона, смотревшего из под руки на флеши. Дым стлался перед флешами, и то казалось, что дым двигался, то казалось, что войска двигались. Слышны были иногда из за выстрелов крики людей, но нельзя было знать, что они там делали.
Наполеон, стоя на кургане, смотрел в трубу, и в маленький круг трубы он видел дым и людей, иногда своих, иногда русских; но где было то, что он видел, он не знал, когда смотрел опять простым глазом.
Он сошел с кургана и стал взад и вперед ходить перед ним.
Изредка он останавливался, прислушивался к выстрелам и вглядывался в поле сражения.
Не только с того места внизу, где он стоял, не только с кургана, на котором стояли теперь некоторые его генералы, но и с самых флешей, на которых находились теперь вместе и попеременно то русские, то французские, мертвые, раненые и живые, испуганные или обезумевшие солдаты, нельзя было понять того, что делалось на этом месте. В продолжение нескольких часов на этом месте, среди неумолкаемой стрельбы, ружейной и пушечной, то появлялись одни русские, то одни французские, то пехотные, то кавалерийские солдаты; появлялись, падали, стреляли, сталкивались, не зная, что делать друг с другом, кричали и бежали назад.
С поля сражения беспрестанно прискакивали к Наполеону его посланные адъютанты и ординарцы его маршалов с докладами о ходе дела; но все эти доклады были ложны: и потому, что в жару сражения невозможно сказать, что происходит в данную минуту, и потому, что многие адъютапты не доезжали до настоящего места сражения, а передавали то, что они слышали от других; и еще потому, что пока проезжал адъютант те две три версты, которые отделяли его от Наполеона, обстоятельства изменялись и известие, которое он вез, уже становилось неверно. Так от вице короля прискакал адъютант с известием, что Бородино занято и мост на Колоче в руках французов. Адъютант спрашивал у Наполеона, прикажет ли он пореходить войскам? Наполеон приказал выстроиться на той стороне и ждать; но не только в то время как Наполеон отдавал это приказание, но даже когда адъютант только что отъехал от Бородина, мост уже был отбит и сожжен русскими, в той самой схватке, в которой участвовал Пьер в самом начале сраженья.
Прискакавший с флеш с бледным испуганным лицом адъютант донес Наполеону, что атака отбита и что Компан ранен и Даву убит, а между тем флеши были заняты другой частью войск, в то время как адъютанту говорили, что французы были отбиты, и Даву был жив и только слегка контужен. Соображаясь с таковыми необходимо ложными донесениями, Наполеон делал свои распоряжения, которые или уже были исполнены прежде, чем он делал их, или же не могли быть и не были исполняемы.
Маршалы и генералы, находившиеся в более близком расстоянии от поля сражения, но так же, как и Наполеон, не участвовавшие в самом сражении и только изредка заезжавшие под огонь пуль, не спрашиваясь Наполеона, делали свои распоряжения и отдавали свои приказания о том, куда и откуда стрелять, и куда скакать конным, и куда бежать пешим солдатам. Но даже и их распоряжения, точно так же как распоряжения Наполеона, точно так же в самой малой степени и редко приводились в исполнение. Большей частью выходило противное тому, что они приказывали. Солдаты, которым велено было идти вперед, подпав под картечный выстрел, бежали назад; солдаты, которым велено было стоять на месте, вдруг, видя против себя неожиданно показавшихся русских, иногда бежали назад, иногда бросались вперед, и конница скакала без приказания догонять бегущих русских. Так, два полка кавалерии поскакали через Семеновский овраг и только что въехали на гору, повернулись и во весь дух поскакали назад. Так же двигались и пехотные солдаты, иногда забегая совсем не туда, куда им велено было. Все распоряжение о том, куда и когда подвинуть пушки, когда послать пеших солдат – стрелять, когда конных – топтать русских пеших, – все эти распоряжения делали сами ближайшие начальники частей, бывшие в рядах, не спрашиваясь даже Нея, Даву и Мюрата, не только Наполеона. Они не боялись взыскания за неисполнение приказания или за самовольное распоряжение, потому что в сражении дело касается самого дорогого для человека – собственной жизни, и иногда кажется, что спасение заключается в бегстве назад, иногда в бегстве вперед, и сообразно с настроением минуты поступали эти люди, находившиеся в самом пылу сражения. В сущности же, все эти движения вперед и назад не облегчали и не изменяли положения войск. Все их набегания и наскакивания друг на друга почти не производили им вреда, а вред, смерть и увечья наносили ядра и пули, летавшие везде по тому пространству, по которому метались эти люди. Как только эти люди выходили из того пространства, по которому летали ядра и пули, так их тотчас же стоявшие сзади начальники формировали, подчиняли дисциплине и под влиянием этой дисциплины вводили опять в область огня, в которой они опять (под влиянием страха смерти) теряли дисциплину и метались по случайному настроению толпы.
Генералы Наполеона – Даву, Ней и Мюрат, находившиеся в близости этой области огня и даже иногда заезжавшие в нее, несколько раз вводили в эту область огня стройные и огромные массы войск. Но противно тому, что неизменно совершалось во всех прежних сражениях, вместо ожидаемого известия о бегстве неприятеля, стройные массы войск возвращались оттуда расстроенными, испуганными толпами. Они вновь устроивали их, но людей все становилось меньше. В половине дня Мюрат послал к Наполеону своего адъютанта с требованием подкрепления.
Наполеон сидел под курганом и пил пунш, когда к нему прискакал адъютант Мюрата с уверениями, что русские будут разбиты, ежели его величество даст еще дивизию.
– Подкрепления? – сказал Наполеон с строгим удивлением, как бы не понимая его слов и глядя на красивого мальчика адъютанта с длинными завитыми черными волосами (так же, как носил волоса Мюрат). «Подкрепления! – подумал Наполеон. – Какого они просят подкрепления, когда у них в руках половина армии, направленной на слабое, неукрепленное крыло русских!»
– Dites au roi de Naples, – строго сказал Наполеон, – qu'il n'est pas midi et que je ne vois pas encore clair sur mon echiquier. Allez… [Скажите неаполитанскому королю, что теперь еще не полдень и что я еще не ясно вижу на своей шахматной доске. Ступайте…]
Красивый мальчик адъютанта с длинными волосами, не отпуская руки от шляпы, тяжело вздохнув, поскакал опять туда, где убивали людей.
Наполеон встал и, подозвав Коленкура и Бертье, стал разговаривать с ними о делах, не касающихся сражения.
В середине разговора, который начинал занимать Наполеона, глаза Бертье обратились на генерала с свитой, который на потной лошади скакал к кургану. Это был Бельяр. Он, слезши с лошади, быстрыми шагами подошел к императору и смело, громким голосом стал доказывать необходимость подкреплений. Он клялся честью, что русские погибли, ежели император даст еще дивизию.
Наполеон вздернул плечами и, ничего не ответив, продолжал свою прогулку. Бельяр громко и оживленно стал говорить с генералами свиты, окружившими его.
– Вы очень пылки, Бельяр, – сказал Наполеон, опять подходя к подъехавшему генералу. – Легко ошибиться в пылу огня. Поезжайте и посмотрите, и тогда приезжайте ко мне.
Не успел еще Бельяр скрыться из вида, как с другой стороны прискакал новый посланный с поля сражения.
– Eh bien, qu'est ce qu'il y a? [Ну, что еще?] – сказал Наполеон тоном человека, раздраженного беспрестанными помехами.
– Sire, le prince… [Государь, герцог…] – начал адъютант.
– Просит подкрепления? – с гневным жестом проговорил Наполеон. Адъютант утвердительно наклонил голову и стал докладывать; но император отвернулся от него, сделав два шага, остановился, вернулся назад и подозвал Бертье. – Надо дать резервы, – сказал он, слегка разводя руками. – Кого послать туда, как вы думаете? – обратился он к Бертье, к этому oison que j'ai fait aigle [гусенку, которого я сделал орлом], как он впоследствии называл его.
– Государь, послать дивизию Клапареда? – сказал Бертье, помнивший наизусть все дивизии, полки и батальоны.