Ферредоксины
Ферредокси́ны (от лат. ferrum — железо; сокращённо обозначается «Фд» ) — группа небольших (6—12 кДа) растворимых белков, содержащих железосерные кластеры и являющихся подвижными переносчиками электронов в ряде метаболических процессов. Обычно они переносят один или два электрона за счёт изменения окисленности атомов железа.
Термин "ферредоксин" был придуман Д. С. Вортоном из химической компании DuPont для обозначения железосодержащего белка, который Мортенсон, Валентайн, и Карнахан выделили из анаэробной бактерии Clostridium pasteurianum в 1962 году[1][2]. В том же году Тагава и Арнон выделили подобный белок из хлоропластов шпината, и назвали его "хлоропластный ферредоксин"[3]. Этот ферредоксин участвует в циклическом и нециклическом транспорте электронов в реакциях фотосинтеза. При нециклическом транспорте, ферредоксин является последним акцептором электронов, а затем окисляется ферментом ферредоксин-НАДФ+-редуктазы[en] (шифр КФ [enzyme.expasy.org/EC/1.18.1.2 1.18.1.2]) , восстанавливая НАДФ+.
К другим биорганическим переносчикам электронов относятся такие группы как рубредоксины, цитохромы, пластоцианины и белки, структурно схожие с белками Риске.
Современная классификация ферредоксинов основана, главным образом, на структуре железосерных кластеров и сравнении белковых последовательностей; принимается во внимание также значение окислительно-восстановительного потенциала и форма спектра поглощения.
Содержание
Fe2S2-ферредоксины
| 2Fe-2S железосерный кластер | |||||||||
| Структура консервативного участка Fe2S2 ферредоксина. | |||||||||
| Идентификаторы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Символ |
Fer2 | ||||||||
| Pfam |
[pfam.xfam.org/family?acc=PF00111 PF00111] | ||||||||
| InterPro |
[www.ebi.ac.uk/interpro/entry/IPR001041 IPR001041] | ||||||||
| PROSITE |
[www.expasy.org/cgi-bin/prosite-search-ac?PDOC00642 PDOC00642] | ||||||||
| SCOP |
[scop.mrc-lmb.cam.ac.uk/scop/search.cgi?tlev=fa;&pdb=3fxc 3fxc] | ||||||||
| SUPERFAMILY |
[supfam.org/SUPERFAMILY/cgi-bin/search.cgi?search_field=3fxc 3fxc] | ||||||||
| OPM protein |
[opm.phar.umich.edu/protein.php?search=1kf6 1kf6] | ||||||||
| |||||||||
Члены семейства 2Fe-2S ферредоксинов имеют базовую белковую структуру, построенную по принципу бета(2)-альфа-бета(2). Сюда относятся путидаредоксин, терпредоксин и адренодоксин[4][5][6][7]. Это белки из приблизительно сотни аминокислот с четырьмя консервативными остатками цистеина, к которым крепится 2Fe-2S кластер. Такой же консервативный домен обнаружен у ряда ферментов и многодоменных белков таких как альдегидоксидоредуктаза (на N-конце), ксантиноксидаза (N-конец), фталатдиоксигеназа (C-конец), в железосерный белок из сукцинатдегидрогеназы (N-конец) и метанмонооксигеназа (N-конец).
Растительные ферредоксины
В первые эту группу белков обнаружили в мембране хлоропластов, откуда она и получило своё название. Характерны для растений и принимают участие в транспорте электронов в ЭТЦ фотосинтеза. В строме хлоропластов ферредоксин выполняется две основные функции: в нециклическом потоке электронов он принимает электрон с железосерного кластера FB, который содержится в фотосистеме I, после чего передаёт его для восстановления НАДФ+ или же возвращает электрон назад в цепь электронного транспорта при циклическом потоке. Восстановленный ферредоксин в хлоропластах используется для восстановления:
- окисленного никотинамидадениндинуклеотидфосфата (НАДФ+) — при участии ферредоксин-НАДФ+-редуктазы (ФНР),
- нитрита в аммоний — при участии нитритредуктазы,
- сульфита в сульфид — при участии сульфитредуктазы,
- и в реакции глутамин + 2-оксоглутарат → 2-глутамат — при участии глутаматсинтазы.
В бактериальной гидроксилирующей дегидрогеназной системе, окисляющей ароматику, они используются как промежуточные переносчики электронов между флавопротеинредуктазой и оксигеназой.
Тиоредоксин-подобные ферредоксины
Fe2S2 ферредоксин из Clostridium pasteurianum (Cp2FeFd) был отнесён к новому белковому семейству на основании его первичной структуры, спектроскопических характеристик его железосерного кластера и уникальной способности заменять два лигирующих остатка цистеина. Хотя физиологическая роль этого ферредоксина остаётся неясной, оказалось, что он специфически взаимодействует с молибден-железным белком нитрогеназы. Были обнаружены и исследованы гомологичные ферредоксины из Azotobacter vinelandii (Av2FeFdI) и Aquifex aeolicus (AaFd). Для ферредоксина AaFd была была получена кристаллическая структура: оказалось, что он существует в форме димера. Сама пространственная структура мономера AaFd отличается от таковой у других Fe2S2 ферредоксинов. Его укладка относится к α+β классу: четыре β-листа и две α-спирали образуют один из вариантов тиоредоксиновой укладки.
Адреноксин-подобные ферредоксины

| Обозначения | |
|---|---|
| Символы | ; FDX |
| Entrez Gene | |
| HGNC | |
| OMIM | |
| RefSeq | |
| UniProt | |
| Другие данные | |
| Локус | 11-я хр., |
В организме человека ферредоксин-1 участвует в синтезе гормонов щитовидной железы. Кроме того, он переносит электроны от адреноксинредуктазы к цитохрому P450, который отщепляет боковую цепь от холестерола. Ферредоксин-1 способен связываться с металлами и белками. Его легко обнаружить в матриксе митохондрий.
Fe4S4- и Fe3S4-ферредоксины
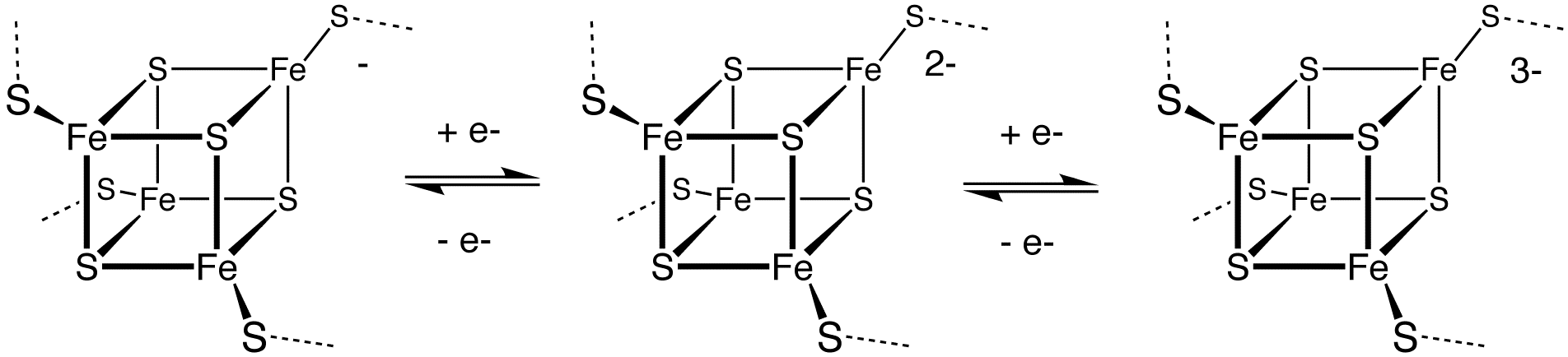
Ферредоксины, содержащие Fe4S4- и Fe3S4-кластеры, характерны для бактерий. Ферредоксины с [Fe4S4] кластером подразделяются на низкопотенциальные (бактериального типа) и высокопотенциальные ферредоксины. Низко- и высокопотенциальные ферредоксины связаны между собой следующей схемой окислительно-восстановительных реакций:
У низкопотенциальных ферредоксинов формальная степень окисления ионов железа может быть [2Fe3+, 2Fe2+] и [1Fe3+, 3Fe2+], а у высокопотенциальных — [3Fe3+, 1Fe2+] или [2Fe3+, 2Fe2+].
Ферредоксины бактериального типа
| 3Fe-4S связывающий домен | |||||||||
 Structural representation of an Fe3S4 ferredoxin. | |||||||||
| Идентификаторы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Символ |
Fer4 | ||||||||
| Pfam |
[pfam.xfam.org/family?acc=PF00037 PF00037] | ||||||||
| InterPro |
[www.ebi.ac.uk/interpro/entry/IPR001450 IPR001450] | ||||||||
| PROSITE |
[www.expasy.org/cgi-bin/prosite-search-ac?PDOC00176 PDOC00176] | ||||||||
| SCOP |
[scop.mrc-lmb.cam.ac.uk/scop/search.cgi?tlev=fa;&pdb=5fd1 5fd1] | ||||||||
| SUPERFAMILY |
[supfam.org/SUPERFAMILY/cgi-bin/search.cgi?search_field=5fd1 5fd1] | ||||||||
| OPM protein |
[opm.phar.umich.edu/protein.php?search=1kqf 1kqf] | ||||||||
| |||||||||
В ходе эволюции ферредоксинов бактериального типа происходили множественные дупликации, транспозиции и слияния генов, в результате чего появились белки сразу с несколькими железосерными кластерами. В некоторых бактериальных ферредоксинах, образовавшиеся в результате удвоения гена домены потеряли один или более консервативный остаток серина. Такие домены либо утратили способность связывать железосерные кластеры либо связываются с [Fe3S4][9] или образуют структуры с двумя кластерами[10].
Для ряда однокластерных и двукластерных членов этой группы известна третичная структура. Их укладка принадлежит к α+β классу, с 2-7 α-спиралями и четырьмя β-листами, которые образуют структуру, напоминающую бета-бочку, и выдающуюся во вне петлю с тремя проксимальными цистеиновыми лигандами железосерного кластера.
Высокопотенциальные железосерные белки
Высокопотенциальный железосерные белки — это уникальное семейство ферредоксинов с Fe4S4 кластером, которые участвуют в анаэробных цепях переноса электронов. У некоторых из них окислительно-восстановительный потенциал выше чем у любого другого белка с железосерным кластером (например, редокс-потенциал белка из Rhodopila globiformis составляет приблизительно 450 мВ)[11]. Для отдельных представителей известна третичная структура: их укладка принадлежит к α+β классу. Как и у остальных бактериальных ферредоксинов их [Fe4S4] кластер обладает кубической структурой и связан с белком через четыре цистеиновых остатка.
Белки человека из семейства ферредоксинов
Напишите отзыв о статье "Ферредоксины"
Примечания
- ↑ Mortenson LE, Valentine RC, Carnahan JE (June 1962). «An electron transport factor from Clostridium pasteurianum». Biochem. Biophys. Res. Commun. 7: 448–52. DOI:10.1016/0006-291X(62)90333-9. PMID 14476372.
- ↑ Valentine RC (December 1964). «Bacterial ferredoxin». Bacteriol Rev 28: 497–517. PMID 14244728.
- ↑ Tagawa K, Arnon DI (August 1962). «Ferredoxins as electron carriers in photosynthesis and in the biological production and consumption of hydrogen gas». Nature 195 (4841): 537–43. DOI:10.1038/195537a0. PMID 14039612. .
- ↑ Jouanneau Y, Armengaud J, Sainz G, Sieker LC (2001). «Crystallization and preliminary X-ray diffraction analysis of a [2Fe-2S] ferredoxin (FdVI) from Rhodobacter capsulatus». Acta Crystallogr. D 57 (Pt 2): 301–303. DOI:10.1107/S0907444900017832. PMID 11173487.
- ↑ Sevrioukova IF (2005). «Redox-dependent Structural Reorganization in Putidaredoxin, a Vertebrate-type [2Fe-2S] Ferredoxin from Pseudomonas putida». J. Mol. Biol. 347 (3): 607–621. DOI:10.1016/j.jmb.2005.01.047. PMID 15755454.
- ↑ Pochapsky TC, Mo H, Pochapsky SS (1999). «A model for the solution structure of oxidized terpredoxin, a Fe2S2 ferredoxin from Pseudomonas». Biochemistry 38 (17): 5666–5675. DOI:10.1021/bi983063r. PMID 10220356.
- ↑ Ruterjans H, Beilke D, Weiss R, Lohr F, Pristovsek P, Hannemann F, Bernhardt R (2002). «A new electron transport mechanism in mitochondrial steroid hydroxylase systems based on structural changes upon the reduction of adrenodoxin». Biochemistry 41 (25): 7969–7978. DOI:10.1021/bi0160361. PMID 12069587.
- ↑ PDB [www.rcsb.org/pdb/explore/explore.do?structureId=3P1M 3P1M]; Chaikuad A, Johansson, C, Krojer, T, Yue, WW, Phillips, C, Bray, JE, Pike, ACW, Muniz, JRC, Vollmar, M, Weigelt, J, Arrowsmith, CH, Edwards, AM, Bountra, C, Kavanagh, K, Oppermann, U (2010). «Crystal structure of human ferredoxin-1 (FDX1) in complex with iron-sulfur cluster». To be published. DOI:10.2210/pdb3p1m/pdb.
- ↑ Fukuyama K, Matsubara H, Katsube Y, Tsukihara T (1989). «Structure of [4Fe-4S] ferredoxin from Bacillus thermoproteolyticus refined at 2.3 A resolution. Structural comparisons of bacterial ferredoxins». J. Mol. Biol. 210 (2): 383–398. DOI:10.1016/0022-2836(89)90338-0. PMID 2600971.
- ↑ Sieker LC, Meyer J, Moulis JM, Fanchon E, Duee ED, Vicat J (1994). «Refined crystal structure of the 2[4Fe-4S] ferredoxin from Clostridium acidurici at 1.84 A resolution». J. Mol. Biol. 243 (4): 683–695. DOI:10.1016/0022-2836(94)90041-8. PMID 7966291.
- ↑ Ambler R. P., Meyer T. E., Kamen M. D. [www.ncbi.nlm.nih.gov/pubmed/8215406 Amino acid sequence of a high redox potential ferredoxin (HiPIP) from the purple phototrophic bacterium Rhodopila globiformis, which has the highest known redox potential of its class.] (англ.) // Archives of biochemistry and biophysics. — 1993. — Vol. 306, no. 1. — P. 215—222. — DOI:10.1006/abbi.1993.1503. — PMID 8215406.
Литература
- Мокроносов А. Т., Гавриленко В. Ф., Жигалова Т. В. Фотосинтез. Физиолого-экологические и биохимические аспекты / под ред. И. П. Ермакова. — 2-е изд., испр. и доп.. — М.: Издательский центр «Академия», 2006. — 448 с. — ISBN 5-7695-2757-9.
Отрывок, характеризующий Ферредоксины
Наташа лежала в постели и в полутьме комнаты рассматривала лицо княжны Марьи.«Похожа она на него? – думала Наташа. – Да, похожа и не похожа. Но она особенная, чужая, совсем новая, неизвестная. И она любит меня. Что у ней на душе? Все доброе. Но как? Как она думает? Как она на меня смотрит? Да, она прекрасная».
– Маша, – сказала она, робко притянув к себе ее руку. – Маша, ты не думай, что я дурная. Нет? Маша, голубушка. Как я тебя люблю. Будем совсем, совсем друзьями.
И Наташа, обнимая, стала целовать руки и лицо княжны Марьи. Княжна Марья стыдилась и радовалась этому выражению чувств Наташи.
С этого дня между княжной Марьей и Наташей установилась та страстная и нежная дружба, которая бывает только между женщинами. Они беспрестанно целовались, говорили друг другу нежные слова и большую часть времени проводили вместе. Если одна выходила, то другаябыла беспокойна и спешила присоединиться к ней. Они вдвоем чувствовали большее согласие между собой, чем порознь, каждая сама с собою. Между ними установилось чувство сильнейшее, чем дружба: это было исключительное чувство возможности жизни только в присутствии друг друга.
Иногда они молчали целые часы; иногда, уже лежа в постелях, они начинали говорить и говорили до утра. Они говорили большей частию о дальнем прошедшем. Княжна Марья рассказывала про свое детство, про свою мать, про своего отца, про свои мечтания; и Наташа, прежде с спокойным непониманием отворачивавшаяся от этой жизни, преданности, покорности, от поэзии христианского самоотвержения, теперь, чувствуя себя связанной любовью с княжной Марьей, полюбила и прошедшее княжны Марьи и поняла непонятную ей прежде сторону жизни. Она не думала прилагать к своей жизни покорность и самоотвержение, потому что она привыкла искать других радостей, но она поняла и полюбила в другой эту прежде непонятную ей добродетель. Для княжны Марьи, слушавшей рассказы о детстве и первой молодости Наташи, тоже открывалась прежде непонятная сторона жизни, вера в жизнь, в наслаждения жизни.
Они всё точно так же никогда не говорили про него с тем, чтобы не нарушать словами, как им казалось, той высоты чувства, которая была в них, а это умолчание о нем делало то, что понемногу, не веря этому, они забывали его.
Наташа похудела, побледнела и физически так стала слаба, что все постоянно говорили о ее здоровье, и ей это приятно было. Но иногда на нее неожиданно находил не только страх смерти, но страх болезни, слабости, потери красоты, и невольно она иногда внимательно разглядывала свою голую руку, удивляясь на ее худобу, или заглядывалась по утрам в зеркало на свое вытянувшееся, жалкое, как ей казалось, лицо. Ей казалось, что это так должно быть, и вместе с тем становилось страшно и грустно.
Один раз она скоро взошла наверх и тяжело запыхалась. Тотчас же невольно она придумала себе дело внизу и оттуда вбежала опять наверх, пробуя силы и наблюдая за собой.
Другой раз она позвала Дуняшу, и голос ее задребезжал. Она еще раз кликнула ее, несмотря на то, что она слышала ее шаги, – кликнула тем грудным голосом, которым она певала, и прислушалась к нему.
Она не знала этого, не поверила бы, но под казавшимся ей непроницаемым слоем ила, застлавшим ее душу, уже пробивались тонкие, нежные молодые иглы травы, которые должны были укорениться и так застлать своими жизненными побегами задавившее ее горе, что его скоро будет не видно и не заметно. Рана заживала изнутри. В конце января княжна Марья уехала в Москву, и граф настоял на том, чтобы Наташа ехала с нею, с тем чтобы посоветоваться с докторами.
После столкновения при Вязьме, где Кутузов не мог удержать свои войска от желания опрокинуть, отрезать и т. д., дальнейшее движение бежавших французов и за ними бежавших русских, до Красного, происходило без сражений. Бегство было так быстро, что бежавшая за французами русская армия не могла поспевать за ними, что лошади в кавалерии и артиллерии становились и что сведения о движении французов были всегда неверны.
Люди русского войска были так измучены этим непрерывным движением по сорок верст в сутки, что не могли двигаться быстрее.
Чтобы понять степень истощения русской армии, надо только ясно понять значение того факта, что, потеряв ранеными и убитыми во все время движения от Тарутина не более пяти тысяч человек, не потеряв сотни людей пленными, армия русская, вышедшая из Тарутина в числе ста тысяч, пришла к Красному в числе пятидесяти тысяч.
Быстрое движение русских за французами действовало на русскую армию точно так же разрушительно, как и бегство французов. Разница была только в том, что русская армия двигалась произвольно, без угрозы погибели, которая висела над французской армией, и в том, что отсталые больные у французов оставались в руках врага, отсталые русские оставались у себя дома. Главная причина уменьшения армии Наполеона была быстрота движения, и несомненным доказательством тому служит соответственное уменьшение русских войск.
Вся деятельность Кутузова, как это было под Тарутиным и под Вязьмой, была направлена только к тому, чтобы, – насколько то было в его власти, – не останавливать этого гибельного для французов движения (как хотели в Петербурге и в армии русские генералы), а содействовать ему и облегчить движение своих войск.
Но, кроме того, со времени выказавшихся в войсках утомления и огромной убыли, происходивших от быстроты движения, еще другая причина представлялась Кутузову для замедления движения войск и для выжидания. Цель русских войск была – следование за французами. Путь французов был неизвестен, и потому, чем ближе следовали наши войска по пятам французов, тем больше они проходили расстояния. Только следуя в некотором расстоянии, можно было по кратчайшему пути перерезывать зигзаги, которые делали французы. Все искусные маневры, которые предлагали генералы, выражались в передвижениях войск, в увеличении переходов, а единственно разумная цель состояла в том, чтобы уменьшить эти переходы. И к этой цели во всю кампанию, от Москвы до Вильны, была направлена деятельность Кутузова – не случайно, не временно, но так последовательно, что он ни разу не изменил ей.
Кутузов знал не умом или наукой, а всем русским существом своим знал и чувствовал то, что чувствовал каждый русский солдат, что французы побеждены, что враги бегут и надо выпроводить их; но вместе с тем он чувствовал, заодно с солдатами, всю тяжесть этого, неслыханного по быстроте и времени года, похода.
Но генералам, в особенности не русским, желавшим отличиться, удивить кого то, забрать в плен для чего то какого нибудь герцога или короля, – генералам этим казалось теперь, когда всякое сражение было и гадко и бессмысленно, им казалось, что теперь то самое время давать сражения и побеждать кого то. Кутузов только пожимал плечами, когда ему один за другим представляли проекты маневров с теми дурно обутыми, без полушубков, полуголодными солдатами, которые в один месяц, без сражений, растаяли до половины и с которыми, при наилучших условиях продолжающегося бегства, надо было пройти до границы пространство больше того, которое было пройдено.
В особенности это стремление отличиться и маневрировать, опрокидывать и отрезывать проявлялось тогда, когда русские войска наталкивались на войска французов.
Так это случилось под Красным, где думали найти одну из трех колонн французов и наткнулись на самого Наполеона с шестнадцатью тысячами. Несмотря на все средства, употребленные Кутузовым, для того чтобы избавиться от этого пагубного столкновения и чтобы сберечь свои войска, три дня у Красного продолжалось добивание разбитых сборищ французов измученными людьми русской армии.
Толь написал диспозицию: die erste Colonne marschiert [первая колонна направится туда то] и т. д. И, как всегда, сделалось все не по диспозиции. Принц Евгений Виртембергский расстреливал с горы мимо бегущие толпы французов и требовал подкрепления, которое не приходило. Французы, по ночам обегая русских, рассыпались, прятались в леса и пробирались, кто как мог, дальше.
Милорадович, который говорил, что он знать ничего не хочет о хозяйственных делах отряда, которого никогда нельзя было найти, когда его было нужно, «chevalier sans peur et sans reproche» [«рыцарь без страха и упрека»], как он сам называл себя, и охотник до разговоров с французами, посылал парламентеров, требуя сдачи, и терял время и делал не то, что ему приказывали.
– Дарю вам, ребята, эту колонну, – говорил он, подъезжая к войскам и указывая кавалеристам на французов. И кавалеристы на худых, ободранных, еле двигающихся лошадях, подгоняя их шпорами и саблями, рысцой, после сильных напряжений, подъезжали к подаренной колонне, то есть к толпе обмороженных, закоченевших и голодных французов; и подаренная колонна кидала оружие и сдавалась, чего ей уже давно хотелось.
Под Красным взяли двадцать шесть тысяч пленных, сотни пушек, какую то палку, которую называли маршальским жезлом, и спорили о том, кто там отличился, и были этим довольны, но очень сожалели о том, что не взяли Наполеона или хоть какого нибудь героя, маршала, и упрекали в этом друг друга и в особенности Кутузова.
Люди эти, увлекаемые своими страстями, были слепыми исполнителями только самого печального закона необходимости; но они считали себя героями и воображали, что то, что они делали, было самое достойное и благородное дело. Они обвиняли Кутузова и говорили, что он с самого начала кампании мешал им победить Наполеона, что он думает только об удовлетворении своих страстей и не хотел выходить из Полотняных Заводов, потому что ему там было покойно; что он под Красным остановил движенье только потому, что, узнав о присутствии Наполеона, он совершенно потерялся; что можно предполагать, что он находится в заговоре с Наполеоном, что он подкуплен им, [Записки Вильсона. (Примеч. Л.Н. Толстого.) ] и т. д., и т. д.
Мало того, что современники, увлекаемые страстями, говорили так, – потомство и история признали Наполеона grand, a Кутузова: иностранцы – хитрым, развратным, слабым придворным стариком; русские – чем то неопределенным – какой то куклой, полезной только по своему русскому имени…
В 12 м и 13 м годах Кутузова прямо обвиняли за ошибки. Государь был недоволен им. И в истории, написанной недавно по высочайшему повелению, сказано, что Кутузов был хитрый придворный лжец, боявшийся имени Наполеона и своими ошибками под Красным и под Березиной лишивший русские войска славы – полной победы над французами. [История 1812 года Богдановича: характеристика Кутузова и рассуждение о неудовлетворительности результатов Красненских сражений. (Примеч. Л.Н. Толстого.) ]
Такова судьба не великих людей, не grand homme, которых не признает русский ум, а судьба тех редких, всегда одиноких людей, которые, постигая волю провидения, подчиняют ей свою личную волю. Ненависть и презрение толпы наказывают этих людей за прозрение высших законов.
Для русских историков – странно и страшно сказать – Наполеон – это ничтожнейшее орудие истории – никогда и нигде, даже в изгнании, не выказавший человеческого достоинства, – Наполеон есть предмет восхищения и восторга; он grand. Кутузов же, тот человек, который от начала и до конца своей деятельности в 1812 году, от Бородина и до Вильны, ни разу ни одним действием, ни словом не изменяя себе, являет необычайный s истории пример самоотвержения и сознания в настоящем будущего значения события, – Кутузов представляется им чем то неопределенным и жалким, и, говоря о Кутузове и 12 м годе, им всегда как будто немножко стыдно.
А между тем трудно себе представить историческое лицо, деятельность которого так неизменно постоянно была бы направлена к одной и той же цели. Трудно вообразить себе цель, более достойную и более совпадающую с волею всего народа. Еще труднее найти другой пример в истории, где бы цель, которую поставило себе историческое лицо, была бы так совершенно достигнута, как та цель, к достижению которой была направлена вся деятельность Кутузова в 1812 году.
Кутузов никогда не говорил о сорока веках, которые смотрят с пирамид, о жертвах, которые он приносит отечеству, о том, что он намерен совершить или совершил: он вообще ничего не говорил о себе, не играл никакой роли, казался всегда самым простым и обыкновенным человеком и говорил самые простые и обыкновенные вещи. Он писал письма своим дочерям и m me Stael, читал романы, любил общество красивых женщин, шутил с генералами, офицерами и солдатами и никогда не противоречил тем людям, которые хотели ему что нибудь доказывать. Когда граф Растопчин на Яузском мосту подскакал к Кутузову с личными упреками о том, кто виноват в погибели Москвы, и сказал: «Как же вы обещали не оставлять Москвы, не дав сраженья?» – Кутузов отвечал: «Я и не оставлю Москвы без сражения», несмотря на то, что Москва была уже оставлена. Когда приехавший к нему от государя Аракчеев сказал, что надо бы Ермолова назначить начальником артиллерии, Кутузов отвечал: «Да, я и сам только что говорил это», – хотя он за минуту говорил совсем другое. Какое дело было ему, одному понимавшему тогда весь громадный смысл события, среди бестолковой толпы, окружавшей его, какое ему дело было до того, к себе или к нему отнесет граф Растопчин бедствие столицы? Еще менее могло занимать его то, кого назначат начальником артиллерии.