Трихлорид азота
Поделись знанием:
Это текущая версия страницы, сохранённая Тара-Амингу (обсуждение | вклад) в 09:47, 19 августа 2016. Вы просматриваете постоянную ссылку на эту версию.
| Трихлорид азота | |
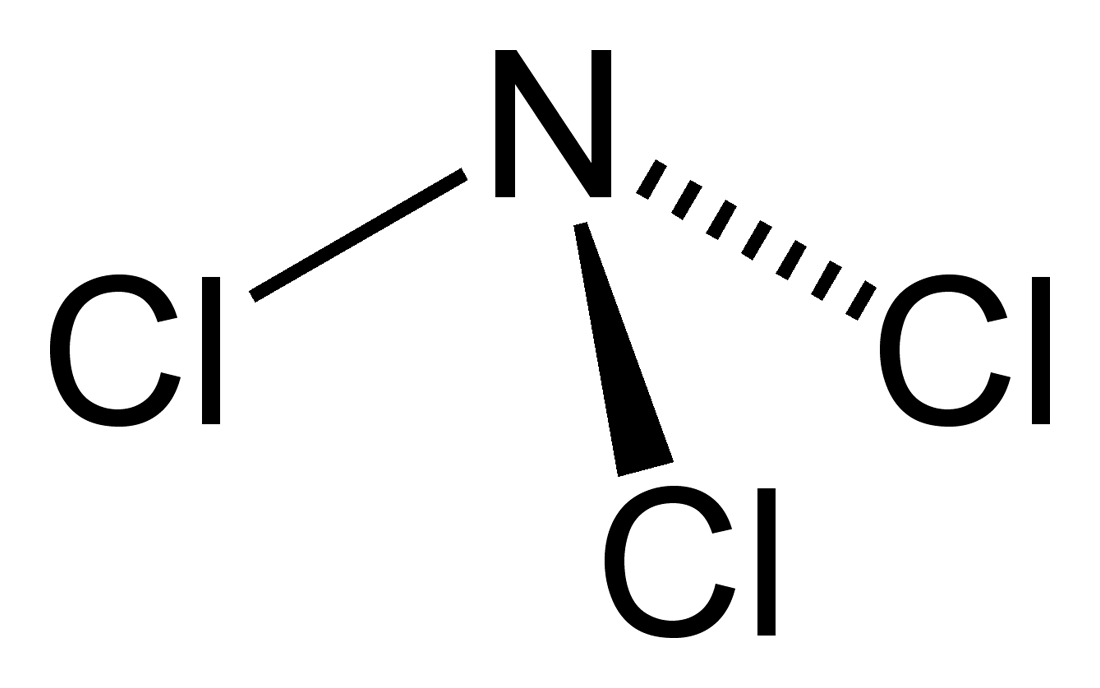
| |
| Nitrogen-trichloride-3D-vdW.png | |
| Общие | |
|---|---|
| Традиционные названия | трихлорид азота, нитрид хлора |
| Хим. формула | NCl3 |
| Физические свойства | |
| Молярная масса | 120.365 г/моль |
| Плотность | 1,635 г/см³ |
| Термические свойства | |
| Т. плав. | −40 °C |
| Т. кип. | 71 °C |
| Классификация | |
| Рег. номер CAS | 10025-85-1 |
| SMILES | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Трихлори́д азо́та (NCl3) — бинарное неорганическое соединение хлора и азота с формулой NCl3, тяжёлая маслянистая летучая жидкость жёлтого цвета.
Получение
Реакция между аммиаком и хлором:
- <math>\mathsf{4NH_3 + 3Cl_2 \rightarrow NCl_3 + 3NH_4Cl}</math>
или солями аммония:
- <math>\mathsf{4NH_4NO_3 + 3Cl_2 \rightarrow NCl_3 + 4HNO_3 + 3NH_4Cl}</math>
Физические свойства
Тяжёлая маслянистая летучая жидкость жёлтого цвета. Растворяется в бензоле, хлороформе, сероуглероде и диэтиловом эфире, плохо растворяется в воде.
В чистом виде при нагреве или ударе взрывается, но менее взрывоопасен, чем сухой трииодид азота. Взрывается при контакте с глицеридами жирных кислот (жирами).
Химические свойства
- Медленно взаимодействует с водой:
- <math>\mathsf{NCl_3 + 3H_2O \rightarrow NH_3 + 3HOCl}</math>
- <math>\mathsf{R_3CH + NCl_3 \rightarrow R_3CNCl_2 + HCl}</math>
- Является сильным ингибитором реакции хлора с водородом, одной тысячной доли процента достаточно для прекращения реакции[1].
Аналоги
- Трииодид азота (NI3)
- Трибромид азота (NBr3)
- Фторид азота(III) (NF3)
Примечания
- ↑ Ингибиторы // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — С. 91. — ISBN 5-7155-0292-6.
| |
Это заготовка статьи о неорганическом веществе. Вы можете помочь проекту, дополнив её. |
